
Wetenschap
Koolstofisotopen:¹²C, ¹³C en ¹⁴C begrijpen
* Koolstof-12 (¹²C) :Dit is de meest voorkomende isotoop van koolstof en vormt ongeveer 98,9% van alle koolstof die in de natuur wordt aangetroffen. Het heeft 6 protonen en 6 neutronen in zijn kern.
* Koolstof-13 (¹³C) :Deze isotoop is minder overvloedig aanwezig en maakt ongeveer 1,1% uit van de natuurlijk voorkomende koolstof. Het heeft 6 protonen en 7 neutronen in zijn kern.
Er is ook een derde, minder voorkomende isotoop:
* Koolstof-14 (¹⁴C) :Dit is een radioactieve isotoop met 6 protonen en 8 neutronen. Het wordt gebruikt voor radiokoolstofdatering, een methode om de ouderdom van organische materialen te bepalen.
Het is belangrijk op te merken dat alle koolstofisotopen hetzelfde aantal protonen (6) hebben, wat hun atoomnummer bepaalt en ze als koolstof definieert. Het verschil ligt in het aantal neutronen dat ze hebben.
Hoofdlijnen
- Celmembraan en homeostase:cellulaire controle begrijpen
- Wat is Linkage Biology?
- Is een bladweefsel of een orgel?
- Het medicijn van mieren:redding en behandeling van gewonde personen
- Wanneer cellen veranderen om verschillende soorten van dat te worden, doen dat banen?
- Welke bacteriën leven en krijgen voeding in uw darmen?
- Wat is het ultieme eindresultaat van glycolyse?
- De natuurkunde laat zien hoe de paddenstoel zijn sporen uitspuugt
- Wat zijn de drie componenten van een operon en hun rollen?
- Hoe pH-veranderingen biologische systemen beïnvloeden

- Wiskunde gebruiken om SARS-CoV-2-eiwitmutaties te voorspellen
- Video:Hoe effectief zijn stoffen maskers tegen het coronavirus?

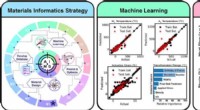
- Nieuwe vormgeheugenlegering ontdekt door middel van kunstmatige intelligentie
- Groen waterzuiveringssysteem werkt zonder zware metalen of bijtende chemicaliën

 Welk element heeft de grotere bindingsenergie -zuurstof of noturogen?
Welk element heeft de grotere bindingsenergie -zuurstof of noturogen?  Een nieuw ontdekte, natuurlijk cafeïnearme theeplant
Een nieuw ontdekte, natuurlijk cafeïnearme theeplant Baramin:Creationistische concepten van biologische classificatie begrijpen
Baramin:Creationistische concepten van biologische classificatie begrijpen  Wat is déjà vu?
Wat is déjà vu?  Chemici ontwerpen mini-ecosystemen om de werking van medicijnen te testen
Chemici ontwerpen mini-ecosystemen om de werking van medicijnen te testen Boskap in Europa bedreigt klimaatdoelen:studie
Boskap in Europa bedreigt klimaatdoelen:studie Termietenheuvels uit de kathedraal inspireren het ontwerp van de maanstructuur
Termietenheuvels uit de kathedraal inspireren het ontwerp van de maanstructuur  Wat is verder de Sun Moon of Star?
Wat is verder de Sun Moon of Star?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


