
Wetenschap
ClF5-hybridisatie:een stapsgewijze handleiding voor het bepalen van de centrale atoomgeometrie
1. Teken de Lewis-structuur:
* Chloor heeft 7 valentie-elektronen.
* Fluor heeft 7 valentie-elektronen.
* Er zijn 5 fluoratomen, dus dat is 5 * 7 =35 valentie-elektronen.
* Totaal valentie-elektronen:7 + 35 =42
* Plaats het chlooratoom in het midden.
* Omring het met 5 fluoratomen.
* Vul de resterende elektronen in om octetten rond de fluoratomen te voltooien.
* Je zult zien dat het centrale chlooratoom vijf bindingen heeft (met de fluoratomen) en één vrij elektronenpaar.
2. Tel het sterische getal:
* Sterisch getal =aantal atomen gebonden aan het centrale atoom + aantal alleenstaande paren op het centrale atoom.
* In ClF5 is het sterische getal 5 + 1 =6.
3. Breng sterisch getal in verband met hybridisatie:
* Sterisch getal van 6 komt overeen met sp³d²-hybridisatie .
Daarom is het centrale chlooratoom in ClF5 sp³d² gehybridiseerd.
Hoofdlijnen
- Hoe is water belangrijk voor de functie van cellen?
- Duurzame biotechnologie werkelijkheid maken:Gebundelde krachten willen biokatalysatoren verbeteren
- Wat is een pluripotentiële stamcel?
- Wat is de eerste stap in wetenschappelijke uitleg?
- Waarom zijn Archegonia en Antheridia tegelijkertijd volwassen op een Prothallus?
- Wat zijn de verschillen tussen een plant en een dierlijke cel onder een microscoop?
- Waar werken een groep vergelijkbare cellen zoals spier in?
- Welk type molecuul biedt cellen met energie - A. koolhydraat B. nucleïnezuur C. Eiwit D. water?
- Hoe cellen in plantenbladeren zichzelf organiseren om een optimaal gebied voor fotosynthese te garanderen
- Bioluminescente worm met ijzeren superkrachten

- Onderzoekers gebruiken supercomputer om inzicht te krijgen in hepatitis B
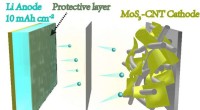
- Chemici vinden nieuwe manier om lithiummetaalelektroden voor batterijen te maken
- Apparaat stuurt sperma tegen de stroom in om onvruchtbaarheid te helpen

- Chemici synthetiseren platte siliciumverbindingen

 Is oceaanwater een zuur of basis?
Is oceaanwater een zuur of basis?  Een elektrische schakelaar voor magnetisme
Een elektrische schakelaar voor magnetisme Wat is het verschil tussen absolute magnitude en helderheid in termen van het meten van de helderheid van hemellichamen?
Wat is het verschil tussen absolute magnitude en helderheid in termen van het meten van de helderheid van hemellichamen?  Een lichtstraal kan worden gezien als het door A paste?
Een lichtstraal kan worden gezien als het door A paste?  Is hetzelfde product gevormd in splijting van uranium 235?
Is hetzelfde product gevormd in splijting van uranium 235?  Wat zijn de atomen van natriumcarbonaat?
Wat zijn de atomen van natriumcarbonaat?  Waarom is Ayers Rock A en niet Mountain?
Waarom is Ayers Rock A en niet Mountain?  Overheden moeten sociale netwerken reguleren:Facebooks Clegg
Overheden moeten sociale netwerken reguleren:Facebooks Clegg
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


