
Wetenschap
Halogenen en edelgassen:overeenkomsten uitgelegd
1. Elektronische configuratie:
* Halogenen hebben zeven valentie-elektronen, één minder dan een volledige buitenschil. Dit maakt ze zeer reactief omdat ze de neiging hebben een elektron te verkrijgen om een stabiele octetconfiguratie te bereiken.
* Edelgassen hebben een volledige buitenste schil van elektronen (behalve Helium, dat een volledige buitenste schil van 2 elektronen heeft). Dit maakt ze zeer stabiel en niet-reactief, omdat ze geen elektronen hoeven te winnen of te verliezen.
2. Niet-metalen eigenschappen:
* Zowel halogenen als edelgassen zijn niet-metalen . Ze zijn over het algemeen slechte geleiders van warmte en elektriciteit en bestaan als gassen bij kamertemperatuur (behalve broom, dat een vloeistof is).
3. Vorming van verbindingen:
* Halogenen vormen gemakkelijk ionische verbindingen door een elektron uit een metaal te halen. Dit komt omdat ze een sterke elektronegativiteit hebben.
* Edelgassen zijn over het algemeen inert en vormen niet gemakkelijk verbindingen. Van sommige zwaardere edelgassen, zoals Xenon en Krypton, is echter aangetoond dat ze onder specifieke omstandigheden verbindingen vormen.
4. Voorkomen in de natuur:
* Zowel halogenen als edelgassen worden in sporenhoeveelheden aangetroffen in de atmosfeer .
* Halogenen worden ook aangetroffen in mineralen en zeewater .
Belangrijkste verschillen:
* Reactiviteit: Halogenen zijn zeer reactief, terwijl edelgassen inert zijn.
* Elektronenaffiniteit: Halogenen hebben hoge elektronenaffiniteiten, terwijl edelgassen zeer lage elektronenaffiniteiten hebben.
* Vorming van verbindingen: Halogenen vormen gemakkelijk verbindingen, terwijl edelgassen alleen onder specifieke omstandigheden verbindingen vormen.
Samenvattend:hoewel halogenen en edelgassen qua reactiviteit sterk verschillen vanwege hun elektronenconfiguraties, delen ze enkele gemeenschappelijke niet-metaalachtige kenmerken en komen ze in de natuur vergelijkbaar voor.
 Tribale stem verwerpt plannen voor ondergrondse opslag van radioactief afval nabij Lake Huron
Tribale stem verwerpt plannen voor ondergrondse opslag van radioactief afval nabij Lake Huron Waarom is kennis van de wetenschap belangrijk voor een schrijver?
Waarom is kennis van de wetenschap belangrijk voor een schrijver?  Wat orkaan Michael ons heeft geleerd over de voorbereiding op het orkaanseizoen van dit jaar
Wat orkaan Michael ons heeft geleerd over de voorbereiding op het orkaanseizoen van dit jaar Wat vindt u in een bosgemeenschap?
Wat vindt u in een bosgemeenschap?  Hoe beïnvloedt precessie de aarde?
Hoe beïnvloedt precessie de aarde?
Hoofdlijnen
- Hoe belangrijk is een vermicultuur?
- Wat is een voorbeeld van biologische technologie?
- Wat is waar aan dieren- en plantencellen tijdens mitose behalve?
- Vogelgriep gedetecteerd bij wilde vogels in New York City
- Welk type zelfstandig naamwoord is bijenkorf?
- Oud DNA brengt ons dichter bij het ontrafelen van geheimen over hoe de moderne mens evolueerde
- Welke term verwijst naar los DNA in een kern?
- Welke organismen die niet hun eigen voedsel kunnen maken, zijn?
- Wanneer het bewijs in een wetenschappelijk experiment geen hypothese ondersteunt, wat moet wetenschappers doen?
- Ziekteverwekkers te slim af zijn - onderzoek is bedoeld om de belangrijkste uitdagingen op het gebied van waterfiltratie op te lossen

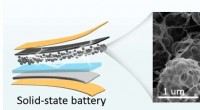
- Hiërarchisch poreuze koolstofnetwerken ingebed met enkele ijzerplaatsen voor efficiënte zuurstofreductie
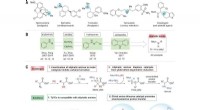
- Een tweestapsbenadering gebruiken om alifatische amines om te zetten in onnatuurlijke aminozuren
- Een nieuwe manier om ijsafzetting te verwijderen zonder stroom of chemicaliën

- Molariteit onder de knie krijgen:een stapsgewijze handleiding voor het berekenen van de molaire concentratie
 Hoeveel bescherming is genoeg?
Hoeveel bescherming is genoeg?  Welke soorten mineralen of gassen worden op de zon gevonden?
Welke soorten mineralen of gassen worden op de zon gevonden?  Welke basis in RNA -paar met adenine?
Welke basis in RNA -paar met adenine?  Hoe het Wallops Command and Data Acquisition Station zich voorbereidt op de lancering van de GOES-T-satelliet
Hoe het Wallops Command and Data Acquisition Station zich voorbereidt op de lancering van de GOES-T-satelliet  Klimaatverandering bedreigt de Moai van Paaseiland
Klimaatverandering bedreigt de Moai van Paaseiland  Wat is vermenigvuldiging?
Wat is vermenigvuldiging?  Ook na handen wassen, nieuwe vingerafdruktest kan onderscheid maken tussen personen die heroïne hebben gebruikt of gebruikt
Ook na handen wassen, nieuwe vingerafdruktest kan onderscheid maken tussen personen die heroïne hebben gebruikt of gebruikt Toegangspatronen verbergen om gevoelige gegevens in de cloud te beschermen
Toegangspatronen verbergen om gevoelige gegevens in de cloud te beschermen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

