
Wetenschap
Ideale gaswet:inzicht in druk, volume, temperatuur en mollen
PV =nRT
waar:
* R is de ideale gasconstante, die een waarde heeft van 8,314 J/mol·K.
Dit is wat de ideale gaswet ons vertelt:
* Directe evenredigheid: De druk van een ideaal gas is recht evenredig met het aantal mol en de temperatuur, en omgekeerd evenredig met het volume.
* Voorspellende kracht: Met de ideale gaswet kunnen we het gedrag van een ideaal gas onder verschillende omstandigheden voorspellen. Als we bijvoorbeeld het volume, de temperatuur en het aantal mol van een gas kennen, kunnen we de druk ervan berekenen.
Belangrijke punten om te onthouden over de ideale gaswet:
* Het is een geïdealiseerd model, wat betekent dat het ervan uitgaat dat gasmoleculen geen volume hebben en geen interactie met elkaar hebben. In werkelijkheid is dit niet helemaal waar, maar de ideale gaswet is een goede benadering voor veel gassen bij lage drukken en hoge temperaturen.
* Dit geldt alleen voor gassen die zich ideaal gedragen. Echte gassen kunnen onder bepaalde omstandigheden afwijken van het ideale gedrag.
Samengevat: De ideale gaswet is een fundamentele vergelijking in de scheikunde en natuurkunde die het gedrag van ideale gassen beschrijft. Het is een krachtig hulpmiddel voor het begrijpen en voorspellen van de eigenschappen van gassen.
 Wat leidt u heel goed met warmte?
Wat leidt u heel goed met warmte?  Naam van binding tussen glucosemoleculen om een polymeer te vormen?
Naam van binding tussen glucosemoleculen om een polymeer te vormen?  Luchtstabiele intrinsiek rekbare kleurconversielagen voor rekbare displays
Luchtstabiele intrinsiek rekbare kleurconversielagen voor rekbare displays Zink of bron? Een nieuw model om organische koolstof in oppervlaktewater te meten
Zink of bron? Een nieuw model om organische koolstof in oppervlaktewater te meten  Wetenschappers hebben de oorsprong van de bouwstenen van het leven ontdekt
Wetenschappers hebben de oorsprong van de bouwstenen van het leven ontdekt
Hoofdlijnen
- Onderzoekers bewerken genen om COVID-19 in het laboratorium te voorkomen en te behandelen. Gaat het werken mensen?
- Welk type cellen bevatten een kern?
- Wat is de wetenschapsdefinitie van onafhankelijke vervalbaar?
- Machine learning classificeert 191 van 's werelds meest schadelijke virussen
- Welke structuur in de kern van eukaryotische cellen heeft DNA gemaakt?
- Wat doet de biosfeer met mensen?
- Zombievirussen op een kapingsreis:hoe retrovirale genfragmenten embryonale cellen beïnvloeden
- Wat zijn de verschillende eigenschappen die wetenschapper over het algemeen bezit?
- Waarom meiose 2 vergelijkbaar is met mitose?
- Wetenschappers ontwerpen veelbelovende nieuwe kathode voor op natrium gebaseerde batterijen

- MRI-techniek detecteert de eigenschappen van verpakt vlees
- Nieuwe algoritmen waarvan is aangetoond dat ze het biofarmaceutische proces versnellen

- Eigenschappen van spinnenzijde geanalyseerd voor gebruik als biogebaseerde vezels in de medische sector

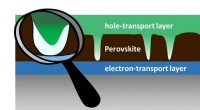
- Perovskiet-zonnecellen:perfectie niet vereist
 Wat is er op de tap? Michigan's economie
Wat is er op de tap? Michigan's economie  Superresolutiemicroscopie:nog dichter bij de limiet komen
Superresolutiemicroscopie:nog dichter bij de limiet komen Supermensen creëren door middel van genmanipulatie en meer
Supermensen creëren door middel van genmanipulatie en meer  Hoe bereken je krachten die op Crank werken?
Hoe bereken je krachten die op Crank werken?  Pure cafeïne extraheren met koffie
Pure cafeïne extraheren met koffie Wat betekent bronnen in een wetenschapsbeursproject?
Wat betekent bronnen in een wetenschapsbeursproject?  Nieuw onderzoek pakt een centrale uitdaging van krachtige quantum computing aan
Nieuw onderzoek pakt een centrale uitdaging van krachtige quantum computing aan Welke wiskundige uitspraak toont de relatie tussen zwaartekracht en massa?
Welke wiskundige uitspraak toont de relatie tussen zwaartekracht en massa?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

