
Wetenschap
Koolstoftetrafluoride (CF₄) vorm:inzicht in de tetraëdrische geometrie
Koolstoftetrafluoride (CF₄) heeft een tetraëdrische vorm.
Dit is waarom:
* Koolstof (C) heeft vier valentie-elektronen.
* Fluor (F) heeft zeven valentie-elektronen.
* Om een stabiel molecuul te vormen, moet koolstof vier elektronen delen, en fluor elk één elektron.
* Dit resulteert in vier enkele bindingen tussen het koolstofatoom en vier fluoratomen.
De vier fluoratomen zijn symmetrisch rond het koolstofatoom gerangschikt en vormen een tetraëder met bindingshoeken van 109,5 °.
 Zijn PCl3 en water oplosbaar, onoplosbaar, mengbaar of niet-mengbaar?
Zijn PCl3 en water oplosbaar, onoplosbaar, mengbaar of niet-mengbaar?  Science Fair-projecten voor longcapaciteit
Science Fair-projecten voor longcapaciteit  Vaccinontwerp kan immuuntherapieën voor kanker drastisch verbeteren
Vaccinontwerp kan immuuntherapieën voor kanker drastisch verbeteren Wat is het massapercentage koolstof in C4H10O?
Wat is het massapercentage koolstof in C4H10O?  Wat is de evenwichtige vergelijking voor natriumnitraatnitriet en zuurstof?
Wat is de evenwichtige vergelijking voor natriumnitraatnitriet en zuurstof?
 Eetbare paddestoelen die op boomschors groeien
Eetbare paddestoelen die op boomschors groeien  Kan de vergissing in het verwoeste majestueuze Kasjmir-meer worden verholpen?
Kan de vergissing in het verwoeste majestueuze Kasjmir-meer worden verholpen?  Waarom kunnen planten niet op de maan groeien?
Waarom kunnen planten niet op de maan groeien?  De diepste meren in de VS:van Crater Lake tot Lake Clark
De diepste meren in de VS:van Crater Lake tot Lake Clark  De aarde heeft nog een paar kansen om catastrofale klimaatverandering te voorkomen. Deze week is er zo een
De aarde heeft nog een paar kansen om catastrofale klimaatverandering te voorkomen. Deze week is er zo een
Hoofdlijnen
- De essentiële rol van bladeren in bonenplanten:fotosynthese en meer
- Verschillen tussen "Fysiek" en "Fysiologisch"
- Waarom zien we cellen zonder microscoop?
- Welke mechanismen leiden tot genetische variatie?
- Welk type reproductie veroorzaakt de meeste diversiteit in nakomelingen?
- Wat zijn de vier klassen van macromoleculen en hun belang?
- Wat is een gereguleerde en begeleide reproductie?
- De overdracht van genetische informatie van ouders op nakomelingen wordt genoemd?
- Wat is het ademhalingssysteem van een kwal?
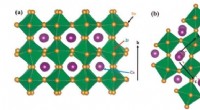
- Diepteafhankelijke valentiestratificatie in een lithiumrijke gelaagde kathode

- Studie onthult unieke fysieke, chemische eigenschappen van cicadevleugels

- Wetenschappers beschrijven de structuur van een toekomstige luminescentiestof

- Pharma streeft naar een betere CBD

- In kaart brengen van het energietransportmechanisme van chalcogenideperovskiet voor gebruik van zonne-energie
 Electron Cloud:atomaire structuur en waarschijnlijkheid begrijpen
Electron Cloud:atomaire structuur en waarschijnlijkheid begrijpen  Specialiteiten van de rechterkant van de hersenen
Specialiteiten van de rechterkant van de hersenen  Wat zijn de voorbeelden van een plant met een zwakke stengel?
Wat zijn de voorbeelden van een plant met een zwakke stengel?  De manier waarop fossielen op zeer droge plaatsen worden gevormd, wordt wat genoemd?
De manier waarop fossielen op zeer droge plaatsen worden gevormd, wordt wat genoemd?  Hoe hangt u onbeweeglijk aan een snaar de krachten beschrijft die op string worden uitgeoefend?
Hoe hangt u onbeweeglijk aan een snaar de krachten beschrijft die op string worden uitgeoefend?  Horizontale Velocity
Horizontale Velocity Heb je het gezien? Supermoon siert de hemel over de hele wereld
Heb je het gezien? Supermoon siert de hemel over de hele wereld  Wat is een natuurlijke factor die soortenbeweging uitblinkt?
Wat is een natuurlijke factor die soortenbeweging uitblinkt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

