
Wetenschap
Niet-polaire opgeloste stoffen:voorbeelden en categorisering - Chemie uitgelegd
Elementen:
* Gassen: Zuurstof (O₂), Stikstof (N₂), Waterstof (H₂), Helium (He), Neon (Ne), Argon (Ar), Krypton (Kr), Xenon (Xe)
* Halogenen: Chloor (Cl₂), Broom (Br₂), Jodium (I₂)
* Vaste niet-metalen: Zwavel (S), Fosfor (P₄), Koolstof (C) (in vormen zoals diamant of grafiet)
Verbindingen:
* Koolwaterstoffen:
* Alkanen: Methaan (CH₄), ethaan (C₂H₆), propaan (C₃H₈), butaan (C₄H₁₀), enz.
* Alkenen: Etheen (C₂H₄), propeen (C₃H₆), buteen (C₄H₈), enz.
* Alkynen: Ethyn (C₂H₂), Propyn (C₃H₄), Butyn (C₄H₆), enz.
* Aromatische koolwaterstoffen: Benzeen (C₆H₆), Tolueen (C₇H₈), Naftaleen (C₁₀H₈), enz.
* Etheren: Diethylether (C₄H₁₀O), dipropylether (C₆H₁₄O), enz.
* Esters: Methylacetaat (C₃H₆O₂), Ethylacetaat (C₄H₈O₂), enz.
* Vetten en oliën: Dit zijn voornamelijk triglyceriden, samengesteld uit glycerol en vetzuren.
* Wassen: Dit zijn esters met lange keten.
* Sommige organische verbindingen: Tetrachloorkoolstof (CCl₄), tetrachloorethyleen (C₂Cl₄), enz.
Belangrijkste punten om te onthouden:
* Niet-polaire opgeloste stoffen zijn meestal samengesteld uit atomen met vergelijkbare elektronegativiteiten, wat leidt tot een evenwichtige verdeling van de elektronendichtheid.
* Ze zijn over het algemeen oplosbaar in niet-polaire oplosmiddelen zoals olie, vet of andere koolwaterstoffen.
* Ze zijn doorgaans hydrofoob (wat betekent dat ze water "vrezen" en er niet gemakkelijk in oplossen).
Laat het me weten als je meer voorbeelden wilt of specifieke categorieën gedetailleerder wilt verkennen.
 Hoe speelt de natuur een rol bij de ontwikkeling van smog?
Hoe speelt de natuur een rol bij de ontwikkeling van smog?  Vrouwen kunnen de dupe worden van de gevolgen van klimaatveranderingen
Vrouwen kunnen de dupe worden van de gevolgen van klimaatveranderingen Braziliaans Amazonegebied registreert minste septemberbranden in 20 jaar
Braziliaans Amazonegebied registreert minste septemberbranden in 20 jaar Nieuwe oliepalmkaart ter informatie van beleid en planning op landschapsniveau
Nieuwe oliepalmkaart ter informatie van beleid en planning op landschapsniveau Iraks Tuin van Eden nu als een woestijn
Iraks Tuin van Eden nu als een woestijn
Hoofdlijnen
- Welke soorten kenmerken gebruiken wetenschappers om levende wezens te classificeren?
- Welke basis wordt normaal gebruikt bij de synthese van RNA maar geen DNA?
- Biology Project Topic voor klasse 12?
- Onshore algenkwekerijen kunnen broodmand worden voor het Zuiden
- Hoe je hersenen werken
- Verouderen bacteriën? Biologen ontdekken dat het antwoord volgt uit eenvoudige economie
- Wat zijn biotische factoren bij varkens?
- Wat beweegt langs het mRNA en helpt peptide -streng te vormen?
- Twee groepen prokaryoten die hun eigen voedsel maken van anorganische moleculen zijn?
- Aniondotering op hoog niveau voor snelle ladingsoverdrachtskinetiek voor condensatoren

- Loden leidingen veilig maken

- Nieuw katalysatormateriaal produceert overvloedige goedkope waterstof

- Waarom zwembadchloor aanzienlijk sterker is dan huishoudbleekmiddel:een gedetailleerde vergelijking

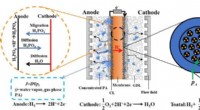
- Het voorspellen van de distributie van fosforzuur en water in een hoge-temperatuur polymeer elektrolytmembraan brandstofcel
 Wat is de formulenaam voor koperen en stikstof?
Wat is de formulenaam voor koperen en stikstof?  Crowdfunding? Check eerst de weersvoorspelling!
Crowdfunding? Check eerst de weersvoorspelling! Hoe afzettingen rijk aan zeldzame aardelementen (REE) in centraal Zweden zijn gevormd
Hoe afzettingen rijk aan zeldzame aardelementen (REE) in centraal Zweden zijn gevormd Innovatieve combinatie van harde en zachte materialen verbetert de hechting op ruwe oppervlakken
Innovatieve combinatie van harde en zachte materialen verbetert de hechting op ruwe oppervlakken Wanneer een fakkel wordt ingeschakeld op energie overgebracht van de batterij naar de lamp Hoe energie?
Wanneer een fakkel wordt ingeschakeld op energie overgebracht van de batterij naar de lamp Hoe energie?  Welk type ecologische piramide volgt het beste de stroom van een ecosysteem?
Welk type ecologische piramide volgt het beste de stroom van een ecosysteem?  Wat is de oxidatietoestand van cupric ion in koperen tartaar-etappe?
Wat is de oxidatietoestand van cupric ion in koperen tartaar-etappe?  Wat is de adellijke gaselektronenconfiguratie voor W?
Wat is de adellijke gaselektronenconfiguratie voor W?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

