
Wetenschap
De impact van kristallen en moleculaire structuren op de eigenschappen van ionische en covalente verbindingen
1. Smeltpunt en kookpunt:
* Ionische verbindingen: Ionische verbindingen hebben sterke elektrostatische aantrekkingen tussen tegengesteld geladen ionen. Deze krachten zijn erg sterk en vereisen veel energie om te overwinnen. Als gevolg hiervan hebben ionische verbindingen hoge smelt- en kookpunten. Ook de rangschikking van ionen in het kristalrooster heeft invloed op deze eigenschappen. Een zeer symmetrisch rooster zoals een face-centered cube (FCC) structuur leidt bijvoorbeeld over het algemeen tot hogere smeltpunten dan een minder symmetrisch rooster.
* Covalente verbindingen: Covalente verbindingen omvatten het delen van elektronen tussen atomen. De sterkte van de intermoleculaire krachten (krachten tussen moleculen) bepaalt hun smelt- en kookpunt.
* Sterkere intermoleculaire krachten: Deze krachten zijn aanwezig in covalente verbindingen zoals waterstofgebonden water, wat resulteert in hogere smelt- en kookpunten.
* Zwakkere intermoleculaire krachten: Covalente verbindingen met zwakkere krachten, zoals de Londense dispersiekrachten, hebben lagere smelt- en kookpunten. Methaan (CH4) heeft bijvoorbeeld een zeer laag kookpunt als gevolg van zwakke intermoleculaire krachten.
2. Oplosbaarheid:
* Ionische verbindingen: Ionische verbindingen zijn meestal oplosbaar in polaire oplosmiddelen zoals water. Dit komt omdat watermoleculen een gedeeltelijke positieve lading op de waterstofatomen en een gedeeltelijke negatieve lading op het zuurstofatoom hebben, waardoor ze met de ionen kunnen interageren en ze uit elkaar kunnen trekken. Ionische verbindingen zijn echter over het algemeen onoplosbaar in niet-polaire oplosmiddelen (zoals olie) omdat de niet-polaire oplosmiddelmoleculen de geladen ionen niet effectief kunnen omringen.
* Covalente verbindingen: Covalente verbindingen lossen over het algemeen op in oplosmiddelen die vergelijkbare intermoleculaire krachten hebben.
* Polaire covalente verbindingen: Polaire covalente verbindingen zoals suiker (glucose) zijn oplosbaar in polaire oplosmiddelen zoals water. Dit komt omdat zowel het oplosmiddel als de opgeloste stof vergelijkbare intermoleculaire krachten hebben.
* Niet-polaire covalente verbindingen: Niet-polaire covalente verbindingen zoals olie zijn oplosbaar in niet-polaire oplosmiddelen zoals benzine. Dit komt omdat de zwakke intermoleculaire krachten (Londense dispersiekrachten) in het oplosmiddel de zwakke intermoleculaire krachten in de opgeloste stof kunnen overwinnen.
Samengevat: De structuur van een verbinding speelt een cruciale rol bij het bepalen van de eigenschappen ervan. Voor ionische verbindingen leiden de sterke elektrostatische krachten als gevolg van het kristalrooster tot hoge smelt-/kookpunten en oplosbaarheid in polaire oplosmiddelen. Voor covalente verbindingen bepaalt de sterkte van de intermoleculaire krachten tussen moleculen hun eigenschappen, waardoor hun smelt-/kookpunten en oplosbaarheid in oplosmiddelen met vergelijkbare intermoleculaire krachten worden beïnvloed.
 Hoe zwarte kinderen op Engelse scholen het gevoel krijgen dat de manier waarop ze spreken verkeerd is
Hoe zwarte kinderen op Engelse scholen het gevoel krijgen dat de manier waarop ze spreken verkeerd is  Hoe maak je de Ethiopische graanschuur klimaatbestendig? Combineer genomics en boerenkennis
Hoe maak je de Ethiopische graanschuur klimaatbestendig? Combineer genomics en boerenkennis  Hoe planten goede buren worden in tijden van stress
Hoe planten goede buren worden in tijden van stress  Hoe beschrijf je de niveaus van organisatie die in je biome leven
Hoe beschrijf je de niveaus van organisatie die in je biome leven  Als het binnenshuis 40°C wordt, is het beter om gebruik te maken van de lokale kennis van de bewoners dan de klimaatverandering van bovenaf te plannen
Als het binnenshuis 40°C wordt, is het beter om gebruik te maken van de lokale kennis van de bewoners dan de klimaatverandering van bovenaf te plannen
Hoofdlijnen
- Wat zijn de belangrijkste fotosynthetische autotrofen in wateromgevingen?
- Wat is de naam van suikermolecule in DNA -necleotiden?
- Welk deel van de wereld heeft een organisme met een hoge dichtheid?
- Kan synthetische biologie wilde dieren redden?
- Wat veroorzaakt psychische aandoeningen?
- Welk type cel is het meest verantwoordelijk voor het doorgeven van informatie aan de hersenen over externe stimuli zoals warmte?
- Welke term beschrijft cellen die slechts één set chromosomen bevatten?
- Waarom zijn mensen koel bloedig?
- Hoe omvat landbouw wetenschap?
- Hybride materiaal kan in verschillende toepassingen beter presteren dan grafeen

- Wetenschappers identificeren potentieel vaccindoelwit voor steeds meer bacteriestammen
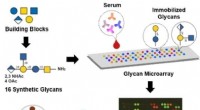
- Interdisciplinaire interacties inspireren nieuwe ontdekkingen

- Bioplottering van bot-mimetische 3D-weefselsteigers met osteogene effecten

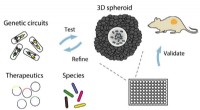
- Onderzoekers ontwikkelen nieuw platform dat kanker in een schaal nabootst om snel de beste bacteriële therapie te bepalen
 Wat is de chemische naam van PT3 (PO3) 4?
Wat is de chemische naam van PT3 (PO3) 4?  Wat is het effect van toevoeging Een katalysator op de chemische reacties van snelheid?
Wat is het effect van toevoeging Een katalysator op de chemische reacties van snelheid?  Vooroordeel in de rockplaat?
Vooroordeel in de rockplaat?  Wat is de helderste ster aan de nachtelijke hemel?
Wat is de helderste ster aan de nachtelijke hemel?  Wat wordt de algemene naam gegeven aan niet -geleidende materialen?
Wat wordt de algemene naam gegeven aan niet -geleidende materialen?  Uit onderzoek blijkt hoe bacteriën in groepen communiceren om antibiotica te vermijden
Uit onderzoek blijkt hoe bacteriën in groepen communiceren om antibiotica te vermijden  2Li begrijpen in de chemie:lithiumatomen uitgelegd
2Li begrijpen in de chemie:lithiumatomen uitgelegd  Wordt de locatie op het oppervlak direct boven het epicentrum van een aardbeving focus genoemd?
Wordt de locatie op het oppervlak direct boven het epicentrum van een aardbeving focus genoemd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

