
Wetenschap
Polaire oplosmiddelen:eigenschappen, kenmerken en voorbeelden
Eigenschappen van een polair oplosmiddel:
Polaire oplosmiddelen hebben verschillende eigenschappen vanwege hun ongelijke verdeling van de elektronendichtheid, wat leidt tot een positief en een negatief uiteinde. Hier is een overzicht:
1. Moleculaire structuur:
* Asymmetrische vorm: Polaire oplosmiddelen hebben een ongelijkmatige verdeling van elektronen binnen hun molecuul, waardoor een dipoolmoment ontstaat. Deze asymmetrie resulteert vaak in gebogen of schuine vormen.
* Polaire bindingen: Ze bevatten bindingen tussen atomen met aanzienlijk verschillende elektronegativiteiten, wat leidt tot een scheiding van ladingen. Voorbeelden zijn onder meer zuurstof-waterstof (O-H) bindingen, stikstof-waterstof (N-H) bindingen en koolstof-zuurstof (C-O) bindingen.
2. Interacties:
* Waterstofbinding: Polaire oplosmiddelen kunnen sterke waterstofbruggen vormen met andere polaire moleculen, waardoor hun eigenschappen zoals kookpunt en oplosbaarheid worden beïnvloed.
* Dipool-dipool-interacties: Ze kunnen interageren met andere polaire moleculen via dipool-dipoolkrachten, wat resulteert in sterkere intermoleculaire krachten vergeleken met niet-polaire oplosmiddelen.
* Ion-dipoolinteracties: Polaire oplosmiddelen kunnen ionische verbindingen oplossen door de positieve en negatieve ionen aan te trekken via elektrostatische interacties.
3. Chemische eigenschappen:
* Hoge diëlektrische constante: Ze hebben een hoge diëlektrische constante, wat betekent dat ze de elektrostatische aantrekkingskracht tussen ionen kunnen verminderen, waardoor het oplossen van ionische verbindingen wordt vergemakkelijkt.
* Goede oplosbaarheid: Ze lossen gemakkelijk polaire moleculen zoals suikers, alcoholen en zouten op vanwege de sterke interacties die ze kunnen vormen.
* Slechte oplosbaarheid van niet-polaire stoffen: Polaire oplosmiddelen kunnen doorgaans niet-polaire stoffen zoals oliën en vetten oplossen.
4. Fysieke eigenschappen:
* Hoog kookpunt: Vanwege de sterke intermoleculaire krachten hebben polaire oplosmiddelen doorgaans hogere kookpunten dan niet-polaire oplosmiddelen.
* Hoge oppervlaktespanning: De sterke interacties tussen polaire moleculen leiden tot een hogere oppervlaktespanning, waardoor ze minder snel verdampen.
Voorbeelden van polaire oplosmiddelen:
* Water (H₂O)
* Ethanol (CH₃CH₂OH)
* Aceton (CH₃COCH₃)
*Dimethylsulfoxide (DMSO)
* Azijnzuur (CH₃COOH)
Belangrijkste afhaalmaaltijden:
Polaire oplosmiddelen worden gekenmerkt door hun vermogen om sterke interacties aan te gaan met andere polaire moleculen en ionen. Hun unieke eigenschappen maken ze geschikt voor het oplossen van polaire stoffen en het faciliteren van chemische reacties waarbij polaire soorten betrokken zijn.
 Hoe chemie een belangrijke rol spelen in je dagelijkse leven?
Hoe chemie een belangrijke rol spelen in je dagelijkse leven?  Wat is de som van de coëfficiënten SF4 plus H20 H2sSO HF?
Wat is de som van de coëfficiënten SF4 plus H20 H2sSO HF?  Welke deeltjes werken samen om atomen zich als vaste stoffen te laten gedragen?
Welke deeltjes werken samen om atomen zich als vaste stoffen te laten gedragen?  Hoe scheid je water en voedselverf?
Hoe scheid je water en voedselverf?  Contrasteren met het vormen en breken van chemische bindingen in termen van energieveranderingen?
Contrasteren met het vormen en breken van chemische bindingen in termen van energieveranderingen?
 Waarom je geen stroman-milieuactivist zou moeten zijn
Waarom je geen stroman-milieuactivist zou moeten zijn Onderzoekers vinden direct bewijs van vingerafdrukken op zeeniveau
Onderzoekers vinden direct bewijs van vingerafdrukken op zeeniveau Ruimtetechnologieën om de milieu- en levensomstandigheden aan de oevers van de Ganges te helpen verbeteren
Ruimtetechnologieën om de milieu- en levensomstandigheden aan de oevers van de Ganges te helpen verbeteren Hoe dood je onkruid rond bomen zonder de boom te kwetsen?
Hoe dood je onkruid rond bomen zonder de boom te kwetsen?  Wat als bomen geen bladeren hadden?
Wat als bomen geen bladeren hadden?
Hoofdlijnen
- Wat wij het doel van wetenschappelijke methode?
- Wat is de wetenschappelijke naam voor het menselijk lichaam?
- Welk orgaan is in de epigastrische regio?
- Welk type aseksuele reproductie is hetzelfde als mitose?
- Wat zijn de voordelen en nadeel van microben?
- Wat betekent het om heterozygoot te zijn voor een eigenschap?
- Wat zijn de verschillende technieken in biotechnologie?
- Wat slaat glycogeen in een cel op?
- Wetenschappers ontdekken aanvallende schimmels die veelbelovend zijn tegen smaragdgroene asboorder
- Biomateriaal kan tand in leven houden na wortelkanaalbehandeling

- Een materiaal ondersteboven keren kan het soms zachter maken

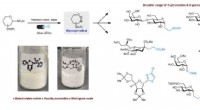
- Activering met zichtbaar licht maakt transformatie van stabiele sulfonen naar waardevolle glycosiden mogelijk
- Wetenschappers vinden frustratie in batterijmaterialen

- Populair nieuw bouwmateriaal helpt bij het meten van eiwitdeeltjes
 Is jouw boterham slecht voor het milieu?
Is jouw boterham slecht voor het milieu?  Wat is de energie van een foton met een golflengte 300 nm?
Wat is de energie van een foton met een golflengte 300 nm?  Welke keuze beschrijft het beste kinetische energie?
Welke keuze beschrijft het beste kinetische energie?  Stappen en procedures voor het uitvoeren van wetenschappelijk onderzoek
Stappen en procedures voor het uitvoeren van wetenschappelijk onderzoek Video:Eclipse-ballonvaartproject
Video:Eclipse-ballonvaartproject Welke vorm van energie heeft een medium nodig om te reizen?
Welke vorm van energie heeft een medium nodig om te reizen?  Wie is de eerste persoon die in de maan is geland?
Wie is de eerste persoon die in de maan is geland?  NASA analyseert zware regenval boven Zuid-Thailand
NASA analyseert zware regenval boven Zuid-Thailand
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

