
Wetenschap
Ionische vaste stoffen in water:oplossing en reacties uitgelegd
1. Ontbinding:
* Oplosbare ionische vaste stoffen: Sommige ionische vaste stoffen zijn oplosbaar in water, wat betekent dat ze oplossen en ionen vormen. Dit gebeurt omdat de sterke elektrostatische aantrekkingskracht tussen de ionen in de vaste stof wordt overwonnen door de aantrekkingskracht tussen de ionen en de polaire watermoleculen. De watermoleculen omringen de ionen, scheiden ze van de vaste stof en zorgen ervoor dat ze vrij in de oplossing kunnen bewegen.
* Voorbeeld: NaCl (keukenzout) lost op in water en vormt Na+ en Cl-ionen.
2. Neerslag:
* Onoplosbare ionische vaste stoffen: Andere ionische vaste stoffen zijn onoplosbaar in water, wat betekent dat ze niet significant oplossen. Dit gebeurt wanneer de aantrekkingskracht tussen de ionen in de vaste stof sterker is dan de aantrekkingskracht tussen de ionen en de watermoleculen.
* Voorbeeld: AgCl (zilverchloride) is onoplosbaar in water en vormt een wit neerslag wanneer het met water wordt gemengd.
3. Evenwicht:
* Enigszins oplosbare ionische vaste stoffen: Sommige ionische vaste stoffen zijn enigszins oplosbaar in water, wat betekent dat een kleine hoeveelheid oplost, maar het grootste deel blijft vast. Hierdoor ontstaat een evenwicht tussen de opgeloste ionen en de vaste stof.
* Voorbeeld: CaCO3 (calciumcarbonaat) is slecht oplosbaar in water. Een kleine hoeveelheid lost op en vormt Ca2+- en CO32--ionen, maar het merendeel van de vaste stof blijft onopgelost.
Factoren die de oplosbaarheid beïnvloeden:
* Roosterenergie: De sterkte van de elektrostatische aantrekkingskracht tussen de ionen in de vaste stof. Hogere roosterenergie betekent een lagere oplosbaarheid.
* Hydratie-energie: De aantrekkingskracht tussen de ionen en de watermoleculen. Hogere hydratatie-energie betekent een hogere oplosbaarheid.
* Temperatuur: Het verhogen van de temperatuur verhoogt gewoonlijk de oplosbaarheid van ionische vaste stoffen.
Andere overwegingen:
* Hydrolyse: Sommige ionische vaste stoffen kunnen met water reageren en nieuwe verbindingen vormen, zoals zuren of basen. Het oplossen van natriumcarbonaat (Na2CO3) in water resulteert bijvoorbeeld in de vorming van carbonaationen (CO32-) die met water kunnen reageren om bicarbonaationen (HCO3-) en hydroxide-ionen (OH-) te vormen, wat resulteert in een basische oplossing.
Samengevat: Het gedrag van ionische vaste stoffen in water is complex en hangt van verschillende factoren af. Het begrijpen van de concepten oplosbaarheid, roosterenergie en hydratatie-energie helpt het lot van een ionische vaste stof te voorspellen wanneer deze in water wordt geplaatst.
 Hoe weet je dat aluminimnfolie een soort dirigent is?
Hoe weet je dat aluminimnfolie een soort dirigent is?  Onderzoeken waarom eigeel werd gebruikt in olieverf van oude meesters
Onderzoeken waarom eigeel werd gebruikt in olieverf van oude meesters  Van de drie soorten radioactiviteit die door Rutherford worden gekenmerkt, welke zijn elektrisch geladen A) B-stralen, B) a-stralen en B-stralen?
Van de drie soorten radioactiviteit die door Rutherford worden gekenmerkt, welke zijn elektrisch geladen A) B-stralen, B) a-stralen en B-stralen?  Wetenschappers maken 3D-geprinte, microscopisch kleine gassensoren:schilderspallets zonder een vleugje pigment
Wetenschappers maken 3D-geprinte, microscopisch kleine gassensoren:schilderspallets zonder een vleugje pigment Wat een hygrometer meet:de vochtigheid en de impact ervan begrijpen
Wat een hygrometer meet:de vochtigheid en de impact ervan begrijpen
 Manilla prullenbak waterweg verstopt met plastic
Manilla prullenbak waterweg verstopt met plastic Wat zijn enkele voorbeelden die soorten beïnvloeden?
Wat zijn enkele voorbeelden die soorten beïnvloeden?  Oceaanalgen krijgen genade van virussen
Oceaanalgen krijgen genade van virussen Puntige aardbevingen voor het gebied van New Madrid:nieuw onderzoek onthult een cluster van gebeurtenissen in het verleden
Puntige aardbevingen voor het gebied van New Madrid:nieuw onderzoek onthult een cluster van gebeurtenissen in het verleden Top 5 gevaarlijkste dieren in Georgië en waar u ze kunt vinden
Top 5 gevaarlijkste dieren in Georgië en waar u ze kunt vinden
Hoofdlijnen
- Welk deel van een cel kan zichzelf kopiëren?
- Ernstig bedreigde vogel met een groter risico om in gevangenschap te worden genomen dan schade te lijden door verlies van leefgebied
- Waarom wordt biotechnologie soms aangeroepen en uitgifte?
- Welke cellen kunnen turgide zijn en waarom?
- Wat is de samenvatting van de procesosmose?
- Vier van de vijf pinyon-jeneverbes boomsoorten die in hun verspreidingsgebied in het westen afnemen
- Wat zijn de verschillende delen van een dierencel?
- Hoe komt osmose voor in cellen?
- Wat is het proces om een eiwit te ontvouwen?
- Wanneer voorspellingen van theoretische chemici werkelijkheid worden

- Instant waterreinigingsmethode miljoenen keren beter dan commerciële aanpak

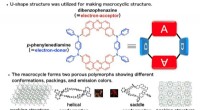
- Unieke organische lichtemitterende moleculaire emitters
- Een thermometer die kan worden uitgerekt en vervormd door water
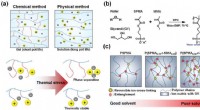
- Iridium-gekatalyseerde waterstofadditie, natuurlijke stoffen op basis van planten en insecten geven

 Wat gebeurt er met de kracht tussen twee ladingen als de omvang van beide wordt verdubbeld en afstand wordt gesneden in tweeën?
Wat gebeurt er met de kracht tussen twee ladingen als de omvang van beide wordt verdubbeld en afstand wordt gesneden in tweeën?  Wat is een geometrische reeks?
Wat is een geometrische reeks?  Welk type omstandigheden ondersteunen de snelle multiplicatiebacteriën?
Welk type omstandigheden ondersteunen de snelle multiplicatiebacteriën?  Het ritme van verandering:wat een drumbeat-experiment onthult over culturele evolutie
Het ritme van verandering:wat een drumbeat-experiment onthult over culturele evolutie  ATLAS Experiment onderzoekt hoe het Higgs-deeltje interageert met andere bosonen
ATLAS Experiment onderzoekt hoe het Higgs-deeltje interageert met andere bosonen  Onderzoekers ontdekken een parallel universum in de tomatengenetica
Onderzoekers ontdekken een parallel universum in de tomatengenetica  Hoe zien we anders dan wolken anders condensatie?
Hoe zien we anders dan wolken anders condensatie?  Wat is de term die wordt gebruikt voor een hoge snelheidsbundel van energie?
Wat is de term die wordt gebruikt voor een hoge snelheidsbundel van energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

