
Wetenschap
Waarom is puur water neutraal?
* Water is een polair molecuul: Het zuurstofatoom in water heeft een enigszins negatieve lading, terwijl de waterstofatomen een enigszins positieve lading hebben. Met deze polariteit kunnen watermoleculen uit elkaar breken en ionen vormen.
* Autoionisatie: Watermoleculen kunnen spontaan met elkaar reageren en een hydroniumion (H3O+) en een hydroxide-ion (OH-) vormen. Dit proces wordt autoionisatie genoemd.
* evenwicht: De autoionisatie van water is een omkeerbare reactie, wat betekent dat het in beide richtingen kan doorgaan. Bij evenwicht is de snelheid van voorwaartse reactie (vorming van ionen) gelijk aan de snelheid van de omgekeerde reactie (recombinatie van ionen).
* Gelijke concentraties: Bij evenwicht is de concentratie van H3O+ -ionen gelijk aan de concentratie van OH-ionen.
* pH -schaal: De pH -schaal meet de zuurgraad of alkaliteit van een oplossing. Een neutrale oplossing heeft een pH van 7. Puur water, met gelijke concentraties van H+ en OH-, heeft een pH van 7, waardoor deze neutraal wordt.
Samenvattend: De neutraliteit van zuiver water komt van de gelijke concentratie van waterstofionen (H+) en hydroxide-ionen (OH-) vanwege het autoionisatieproces, dat een pH van 7 handhaaft.
 Onderzoekers onthullen hoe mycorrhiza-soorten de koolstof in de plantenbodem in bossen reguleren
Onderzoekers onthullen hoe mycorrhiza-soorten de koolstof in de plantenbodem in bossen reguleren  Nieuwe infrageluidsensorarray van Sandia detecteert explosies
Nieuwe infrageluidsensorarray van Sandia detecteert explosies Hoe de veerkracht van een gemeenschap te beoordelen
Hoe de veerkracht van een gemeenschap te beoordelen  Wat is de natuurlijke selectie ook bekend als?
Wat is de natuurlijke selectie ook bekend als?  Organismen met kleine genomen, cellen die gedijen in hete bodems
Organismen met kleine genomen, cellen die gedijen in hete bodems
Hoofdlijnen
- Welke variabele heeft geen invloed op de biome -verdeling?
- Kunt u Archaea en Eubacteria identificeren of classificeren?
- Wat zijn enkele voorbeelden van interne ontwikkeling?
- Wat is de functie, heeft het vetweefsel in vetten?
- G2-fase: wat gebeurt er in deze subfase van de celcyclus?
- Welk bloedgroep brengt zuurstof dicht bij cellen?
- Hoe zorgt de structurele organisatie van membranen voor transport en erkenning?
- Wetenschappers kunnen zien of organismen nauw verwant zijn door hun te vergelijken?
- Wat houden gameten om het chromosoomaantal van een organisme te behouden?
- Gewasafval omzetten in hoogwaardige modeproducten

- Nieuwe strategie voor afgifte van therapeutische eiwitten kan helpen bij de behandeling van degeneratieve oogziekten
- Wetenschappers verduidelijken aspect van interacties tussen vaste stoffen en vloeistoffen in dunne film

- Nieuwe lijm voor betere recycling

- Gastuitlijning en defectvorming tijdens porievulling in metaal-organische raamwerkfilms
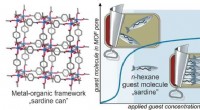
 Slim medicijnontwerp om resistentie tegen malariabehandeling te voorkomen
Slim medicijnontwerp om resistentie tegen malariabehandeling te voorkomen Welk materiaal is een vloeistof bij kamertemperatuur 25c?
Welk materiaal is een vloeistof bij kamertemperatuur 25c?  Bikini-atol in kaart brengen
Bikini-atol in kaart brengen Is geconcentreerde energie nuttiger dan verspreiding van energie?
Is geconcentreerde energie nuttiger dan verspreiding van energie?  Het bevruchte ei van een mens bevat hoeveel chromosomen?
Het bevruchte ei van een mens bevat hoeveel chromosomen?  Onderzoekers bedenken een theoretische beschrijving van door licht geïnduceerde topologische toestanden
Onderzoekers bedenken een theoretische beschrijving van door licht geïnduceerde topologische toestanden Geneesmiddelkandidaat krimpt tumor wanneer het wordt afgeleverd door nanodeeltjes van plantenvirus
Geneesmiddelkandidaat krimpt tumor wanneer het wordt afgeleverd door nanodeeltjes van plantenvirus Welk molecuul wordt gevonden in DNA maar geen RNA?
Welk molecuul wordt gevonden in DNA maar geen RNA?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

