
Wetenschap
Wordt een watermolecuul beschreven als polair of niet en waarom?
* Ongelijke delen van elektronen: Het zuurstofatoom in water is meer elektronegatief dan de waterstofatomen. Dit betekent dat het de gedeelde elektronen in de covalente bindingen sterker aantrekt. Dit resulteert in het zuurstofatoom met een enigszins negatieve lading (δ-) en de waterstofatomen met enigszins positieve ladingen (Δ+).
* gebogen moleculaire vorm: Het watermolecuul heeft een gebogen vorm, zoals een V. Deze vorm, samen met de ongelijke elektronenverdeling, creëert een scheiding van lading in het molecuul. De zuurstofzijde heeft een negatieve pool en de waterstofzijde heeft een positieve pool.
Samenvattend komt de polariteit van een watermolecuul voort uit zijn asymmetrische vorm en de ongelijke delen van elektronen tussen de zuurstof- en waterstofatomen.
 Wat zijn 5 abiotische factoren die het ecosysteem van Saguaro National Park beïnvloeden en waarom?
Wat zijn 5 abiotische factoren die het ecosysteem van Saguaro National Park beïnvloeden en waarom?  Om de opwarming tot 2 graden Celsius te beperken, zijn emissiereducties in het hele voedselsysteem nodig
Om de opwarming tot 2 graden Celsius te beperken, zijn emissiereducties in het hele voedselsysteem nodig De seismische zone verontrustend door aardbeving getroffen Mexico
De seismische zone verontrustend door aardbeving getroffen Mexico Wat is gemeen door ijskoud water?
Wat is gemeen door ijskoud water?  Wat zijn de voorbeelden van fysieke veranderingen in lucht en land?
Wat zijn de voorbeelden van fysieke veranderingen in lucht en land?
Hoofdlijnen
- Hoe heet een ontwikkeld embryo?
- Wat is de belangrijkste familie van voedselproducerende planten?
- Om een kenmerk van de ene soort over te dragen, is het noodzakelijk transfe?
- Welke term definieert vraag over wat mensen doen met de kennis in de biologie die niet kan worden beantwoord met behulp van de wetenschappelijke methode?
- Geef de fasen in het proces van bevruchtingszoogdieren?
- Wat is de grootte van het menselijk genoom?
- Wat zijn de N bevattende basen van DNA?
- Wat is de term die wordt gebruikt om de verspreiding van ongewenste microben te beschrijven?
- Hoe boerderijen kunnen helpen het microbioom van de aarde te verdedigen
- Nieuw biomateriaal kan plastic laminaten vervangen, sterk verminderen vervuiling

- Het geheim van hernieuwbare zonnebrandstoffen is een af-en-aan relatie

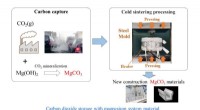
- Het nabootsen van de aardkorst:onderzoek naar de stolling van kandidaten voor bouwmaterialen door koud sinteren
- Het identificeren van designer medicijnen die worden ingenomen door patiënten met een overdosis

- Vooruitgang in het begrip van volledig solid-state batterijen
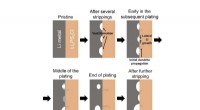
 Direct bewijs van gescheiden oceanische korst gevangen in de overgangszone van de mantel
Direct bewijs van gescheiden oceanische korst gevangen in de overgangszone van de mantel Het geheim van 3D-grafeen? Vries het gewoon in
Het geheim van 3D-grafeen? Vries het gewoon in Simulaties van de inslagkrater laten zien dat kleine asteroïden waarschijnlijk jong zijn
Simulaties van de inslagkrater laten zien dat kleine asteroïden waarschijnlijk jong zijn  Nieuwe techniek bepaalt nauwkeuriger de leeftijd van sterren
Nieuwe techniek bepaalt nauwkeuriger de leeftijd van sterren Realisatie van kleurfiltervrije beeldsensoren
Realisatie van kleurfiltervrije beeldsensoren Solar Orbiter maakt eerste dichte nadering van de zon
Solar Orbiter maakt eerste dichte nadering van de zon Welke Joviaanse planeet heeft geen ringen?
Welke Joviaanse planeet heeft geen ringen?  Welke veranderingen in beweging kunnen een veranderingssnelheid tot gevolg hebben?
Welke veranderingen in beweging kunnen een veranderingssnelheid tot gevolg hebben?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

