
Wetenschap
Hoe zijn twee isotopen van een anders element?
Hier is een uitsplitsing:
* element: Gedefinieerd door het aantal protonen in zijn kern. Alle atomen van een specifiek element hebben hetzelfde aantal protonen.
* isotopen: Atomen van hetzelfde element met verschillende aantallen neutronen . Dit betekent dat ze hetzelfde atoomnummer hebben (aantal protonen) maar verschillende atoommassa (aantal protonen + neutronen).
Hier is een voorbeeld:
* carbon-12 heeft 6 protonen en 6 neutronen.
* carbon-14 heeft 6 protonen en 8 neutronen.
Beide zijn koolstofatomen (omdat ze 6 protonen hebben), maar ze hebben verschillende aantallen neutronen. Dit verschil in neutronentelling maakt hen isotopen.
Key Takeaways:
* Isotopen van hetzelfde element hebben dezelfde chemische eigenschappen omdat ze hetzelfde aantal elektronen hebben, die bepalen hoe een atoom interageert met andere atomen.
* Isotopen kunnen verschillende fysische eigenschappen hebben, zoals dichtheid en radioactieve vervalpercentages, vanwege het verschillende aantal neutronen.
 Het kan zijn dat u meer kleine nanodeeltjes uit uw gasfornuis inademt dan uit de uitlaatgassen van uw auto
Het kan zijn dat u meer kleine nanodeeltjes uit uw gasfornuis inademt dan uit de uitlaatgassen van uw auto  Waarom worden vissen als een natuurlijke hulpbron beschouwd?
Waarom worden vissen als een natuurlijke hulpbron beschouwd?  Planten en dieren die leven in de buurt van de Koalas Habitat
Planten en dieren die leven in de buurt van de Koalas Habitat Wat zijn de 3 delen van de biosfeer?
Wat zijn de 3 delen van de biosfeer?  Tsjechen maken een 3D-print van de Eiffeltoren van oceaanafval voor de Olympische Spelen
Tsjechen maken een 3D-print van de Eiffeltoren van oceaanafval voor de Olympische Spelen
Hoofdlijnen
- Bepaalde oogstamcellen kunnen alleen differentiëren in enkele soorten cellen. Wat voor soort cel is dit?
- Ziek van de Mexicaanse griep? Giftige algen kunnen de volgende grote bedreiging zijn
- Is het waar dat sommige bacteriën geen ziekteverwekkers zijn?
- Hoe classificeren aboringinale mensen organismen?
- Onderzoekers ontleden het DNA van 's werelds grootste zoogdieren om te ontdekken hoe walvissen de kans op kanker trotseren
- Zien hoe evolutionaire mechanismen biologische diversiteit opleveren
- Wat bepaalt de eigenschappen van een organisme in DNA?
- Archaea kan kieskeurige eters zijn:onderzoek toont aan dat een groep parasitaire microben het metabolisme van de gastheer kan veranderen
- Wat is het voedselweb van een toucan?
- Geconjugeerde polymeren verbeteren massaspectrometrie en beeldvorming
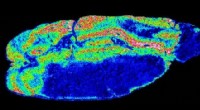
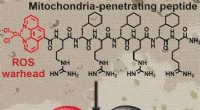
- Een metallopeptide richt zich op en verstoort de mitochondriale functie in stamcellen van borstkanker
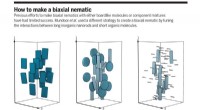
- Een nieuwe manier om biaxiale vloeibare kristallen in nematische fase te maken
- Monolithische nanokoolstofkatalysatoren starten selectieve oxidatie van diwaterstofsulfide

- Fotokatalysator bij lage temperatuur kan de ecologische voetafdruk van syngas verkleinen

 Wat is de term die wordt gebruikt voor proces waarin stralende energie wordt omgezet in potentiële energie?
Wat is de term die wordt gebruikt voor proces waarin stralende energie wordt omgezet in potentiële energie?  Geheimzinnige doelen voor bonussen van CEO's wijzen op slechte prestaties
Geheimzinnige doelen voor bonussen van CEO's wijzen op slechte prestaties YouTube om gezaghebbende virusinhoud op de startpagina te promoten
YouTube om gezaghebbende virusinhoud op de startpagina te promoten Wat is de wetenschappelijke naam van op olie gebaseerde klei?
Wat is de wetenschappelijke naam van op olie gebaseerde klei?  Wat is marmer dat ooit sedimentair rots werd genoemd?
Wat is marmer dat ooit sedimentair rots werd genoemd?  Hoe kunt u stoffen van verschillende dichtheden scheiden?
Hoe kunt u stoffen van verschillende dichtheden scheiden?  Hoe lactoferrine de vrij rondlopende ijzerionen klemt om schadelijke effecten op cellen te stoppen
Hoe lactoferrine de vrij rondlopende ijzerionen klemt om schadelijke effecten op cellen te stoppen Groupie-sterrenstelsels in een baan om de Melkweg vertellen ons over donkere materie, hoe de melkweg is gevormd
Groupie-sterrenstelsels in een baan om de Melkweg vertellen ons over donkere materie, hoe de melkweg is gevormd
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

