
Wetenschap
Waarom zijn niet -metalen goede isolatoren?
* valentie -elektronen: Niet -metalen hebben meestal een groot aantal valentie -elektronen (elektronen in de buitenste schaal). Deze elektronen zijn strak gebonden aan de kern en zijn niet gemakkelijk losgemaakt.
* energiekloven: De energiekloof tussen de valentieband (waar elektronen verblijven) en de geleidingsband (waar elektronen vrij kunnen bewegen) in niet -metalen is groot. Dit betekent dat er veel energie nodig is om een elektron van de valentieband op te wekken naar de geleidingsband, waardoor het voor elektronen moeilijk is om te stromen.
* Covalente binding: Veel niet -metalen vormen sterke covalente bindingen, waarbij elektronen worden gedeeld tussen atomen. Dit delen van elektronen leidt tot een meer rigide structuur met minder vrije elektronen beschikbaar voor geleiding.
metalen zijn daarentegen goede geleiders omdat:
* Ze hebben losjes valentie -elektronen vastgehouden die gemakkelijk door het materiaal kunnen bewegen.
* Hun energiekloof tussen valentie- en geleidingsbanden is erg klein, waardoor elektronen vrij kunnen bewegen met minimale energie -input.
Samenvattend: De strak gebonden elektronen van niet -metalen, grote energiekloven en sterke covalente bindingen beperken de beweging van elektronen, waardoor ze slechte geleiders en uitstekende isolatoren zijn.
 Wat is een dirigent dat metaal?
Wat is een dirigent dat metaal?  Tweedimensionaal MXene als nieuw elektrodemateriaal voor weergave van de volgende generatie
Tweedimensionaal MXene als nieuw elektrodemateriaal voor weergave van de volgende generatie Ontdekking kan microverontreinigingen uit het milieu verwijderen
Ontdekking kan microverontreinigingen uit het milieu verwijderen Wat zijn de verschillende zuurstoftanks met kleurcoderingen en welke betekenis hebben hun kleuren?
Wat zijn de verschillende zuurstoftanks met kleurcoderingen en welke betekenis hebben hun kleuren?  Heliumfusie resulteert in de productie van?
Heliumfusie resulteert in de productie van?
 Wat is het doel van Luna-motten?
Wat is het doel van Luna-motten?  Broeikasgasgegevens diepe duik bereikt nieuw niveau van redelijk en waar
Broeikasgasgegevens diepe duik bereikt nieuw niveau van redelijk en waar Verbeterde opbrengsten in Afrikaanse projectgebieden
Verbeterde opbrengsten in Afrikaanse projectgebieden Bomen in dit biome werpen hun bladeren af. De herfsttemperatuur varieert met seizoenen is de?
Bomen in dit biome werpen hun bladeren af. De herfsttemperatuur varieert met seizoenen is de?  Het bos ruiken, geen bomen:waarom dieren beter zijn in het opsnuiven van complexe geuren
Het bos ruiken, geen bomen:waarom dieren beter zijn in het opsnuiven van complexe geuren
Hoofdlijnen
- De groeiherstel Het gebruik van voedsel in uw lichaam is welk deelcelproces?
- Welke organel- of celstructuur zou je verwachten dat deze de meeste radioactiviteit bevat na een DNA-synthese?
- Hoe betrouwbaar zijn schildpadden voor het meten van afval in de oceaan en de gezondheid van de zee?
- Bewijs van de activiteitenorganismen in het verleden wordt een genoemd?
- Welke andere gegevens naast fysieke kenmerken gebruiken wetenschappers om te vinden of organismen gerelateerd zijn?
- Voor welk type dosisgenen van molecuul coderen ze voor?
- Wat is de oorsprong van het leven op aarde?
- Wat kan veranderingen in DNA -sequenties veroorzaken?
- Zijn krokodillen geheime fruitliefhebbers?
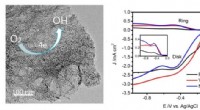
- Nieuwe elektrokatalysator ontwikkeld voor zuurstofreductiereactie
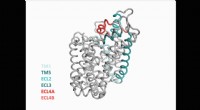
- Wetenschappers gebruiken chemische hulpmiddelen om kankerverwekkende eiwitten op te sporen

- Nobelprijswinnende techniek zoals Google Earth voor moleculen

- Röntgenbeeldvorming onthult inzichten in een natuurlijke mug-dodende verbinding

- Neurowetenschappers ontdekken nieuwe structuur van belangrijk eiwit in de hersenen
 Hoe warmere wateren als gevolg van klimaatverandering de biochemie en de groei van vissen beïnvloeden
Hoe warmere wateren als gevolg van klimaatverandering de biochemie en de groei van vissen beïnvloeden  Wat is de snelheid waarmee energie is omgezet?
Wat is de snelheid waarmee energie is omgezet?  Waarom stinkt de stinkplant?
Waarom stinkt de stinkplant?  Een Amerikaanse satelliet met een massa van 20000 kg ligt op 40 meter van een vijand 15000 Wat de zwaartekracht tussen hen?
Een Amerikaanse satelliet met een massa van 20000 kg ligt op 40 meter van een vijand 15000 Wat de zwaartekracht tussen hen?  Waarom zijn sommige tapes plakkeriger dan andere?
Waarom zijn sommige tapes plakkeriger dan andere?  Hoe beïnvloedt een bosbrand levende en niet-levende dingen?
Hoe beïnvloedt een bosbrand levende en niet-levende dingen?  Lab verandert fluorescerende tags in kankermoordenaars
Lab verandert fluorescerende tags in kankermoordenaars Wat doen geowetenschappers dat andere wetenschappers doen?
Wat doen geowetenschappers dat andere wetenschappers doen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

