
Wetenschap
Hoeveel moleculen zijn er in 654,5 gram calciumchloride?
Hier leest u hoe u het aantal moleculen in 654,5 gram calciumchloride (CaCl₂) kunt berekenen:
1. Vind de molaire massa van CaCl₂:
* CA:40.08 g/mol
* Cl:35,45 g/mol (x 2 voor twee chlooratomen)
* Totale molaire massa =40,08 + (35,45 x 2) =110,98 g/mol
2. Converteer grams naar mollen:
* Mol =(gram) / (molaire massa)
* Mol =654,5 g / 110,98 g / mol
* Mol ≈ 5.89 mol
3. Gebruik het nummer van Avogadro om het aantal moleculen te vinden:
* Avogadro's nummer =6.022 x 10²³ Moleculen/mol
* Aantal moleculen =(mol) x (Avogadro's nummer)
* Aantal moleculen ≈ 5,89 mol x 6,022 x 10²³ Moleculen/mol
* Aantal moleculen ≈ 3,55 x 10²⁴ moleculen
Daarom zijn er ongeveer 3,55 x 10²⁴ moleculen in 654,5 gram calciumchloride.
 Nieuw soort interactie ontdekt in waterstofproducerende enzymen
Nieuw soort interactie ontdekt in waterstofproducerende enzymen 4D-geprint thermiet kan lassen in de ruimte en gevechtszones gemakkelijker maken, veiliger
4D-geprint thermiet kan lassen in de ruimte en gevechtszones gemakkelijker maken, veiliger Hoeveel atomen zijn er in 4SO2?
Hoeveel atomen zijn er in 4SO2?  Nieuwe materialen om branden in lithium-ionbatterijen te helpen stoppen, explosies en de prestaties van de batterij verbeteren
Nieuwe materialen om branden in lithium-ionbatterijen te helpen stoppen, explosies en de prestaties van de batterij verbeteren Bij 115 graden verandert zwavel in A?
Bij 115 graden verandert zwavel in A?
 Waarom moet je de wetenschappelijke houding bezitten?
Waarom moet je de wetenschappelijke houding bezitten?  Wat is het meest voorkomende element in de oceaan?
Wat is het meest voorkomende element in de oceaan?  Luchtvervuiling heeft mogelijk het verlies van zee-ijs in het midden van de 20e eeuw gemaskeerd
Luchtvervuiling heeft mogelijk het verlies van zee-ijs in het midden van de 20e eeuw gemaskeerd NASA biedt een infraroodanalyse van tyfoon Halong
NASA biedt een infraroodanalyse van tyfoon Halong Door vliegers geblazen Antarctische ontdekkingsreizigers maken de meest zuidelijke positie van Galileo vast
Door vliegers geblazen Antarctische ontdekkingsreizigers maken de meest zuidelijke positie van Galileo vast
Hoofdlijnen
- Wat is de naam van een groep anders weefsel dat samenwerkt?
- Sociale vleermuizen betalen een prijs:schimmelziekte, witte-neussyndroom... uitsterven?
- De lange en korte van een supergen voor efficiënte bestuiving
- Wat doet de gladde ER in een dierencel?
- Waarom zijn er geen zeeslangen in de Atlantische Oceaan?
- Kenmerken levende cel
- Bij herhaling:Biologen observeren in de loop van de tijd terugkerende evolutionaire veranderingen bij wandelende takken
- Tijm tussen amandelbomen verzacht de klimaatverandering en verhoogt de landproductie
- In welke staten dat elk genpaar onafhankelijk van de paren wordt geërfd voor andere eigenschappen?
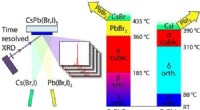
- Krachtige zonnecellen:natuurkundigen kweken stabiele perovskietlagen
- Koolstof vertoont kwantumeffecten

- Monitoring van COVID-19:kunnen medicijnen gevonden in afvalwater een vroege waarschuwing geven?

- Onderzoekers voegen orde toe aan polymeergels

- Oesterschelpen inspireren nieuwe methode om supersterke, flexibele polymeren

 Onderzoeker:Ik heb moeders met vijf of meer kinderen geïnterviewd – wat heb ik geleerd over vrouwen die stilletjes tegen de stroom ingaan
Onderzoeker:Ik heb moeders met vijf of meer kinderen geïnterviewd – wat heb ik geleerd over vrouwen die stilletjes tegen de stroom ingaan  Hoe lang nog tot efficiënte brandstofcellen? Vraag het de experts
Hoe lang nog tot efficiënte brandstofcellen? Vraag het de experts Hoe vermijden trekvogels roofdieren tijdens het tanken?
Hoe vermijden trekvogels roofdieren tijdens het tanken?  Vitale infrastructuren in Nederland kwetsbaar voor hackers
Vitale infrastructuren in Nederland kwetsbaar voor hackers Waarom vormen bacteriën die sporen vormen een groter gezondheidsrisico dan die sporen?
Waarom vormen bacteriën die sporen vormen een groter gezondheidsrisico dan die sporen?  AC-spanning omzetten naar DC
AC-spanning omzetten naar DC Wat zit er in chili of azijn die insecten doden?
Wat zit er in chili of azijn die insecten doden?  Welk type kristallijne structuur bezit Cobalt?
Welk type kristallijne structuur bezit Cobalt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

