
Wetenschap
Hoe weet u wanneer een chemische reactie is afgelopen?
1. Fysieke veranderingen observeren:
* kleurverandering: Als de reactanten en producten verschillende kleuren hebben, kan de kleurverandering de voltooiing van de reactie aangeven.
* Vorming van neerslag: Als een solide vormt uit de oplossing, geeft dit de vorming van een nieuw product aan en kan de reactie eindigen.
* Gasevolutie: Als bubbels ontstaan, betekent dit dat gas wordt vrijgegeven, wat aangeeft dat de reactie aan de gang is. Het beëindigen van borrelen suggereert voltooiing.
* Temperatuurverandering: Sommige reacties geven warmte vrij (exotherme) en worden warmer, terwijl anderen warmte absorberen (endotherm) en kouder worden. De temperatuurverandering kan de voortgang van de reactie aangeven.
2. Monitoring van chemische eigenschappen:
* pH -verandering: Reacties met zuren en basen resulteren vaak in pH -veranderingen. Monitoring van de pH kan de voltooiing van de reactie aangeven.
* Geleidbaarheidsverandering: Het vermogen van een oplossing om elektriciteit te leiden kan tijdens een reactie veranderen. Dit kan wijzen op de vorming van nieuwe ionen of het verdwijnen van bestaande.
3. Instrumenten gebruiken:
* spectrofotometer: Meet de hoeveelheid licht geabsorbeerd of overgedragen door een stof, die kan worden gebruikt om de concentratie van reactanten of producten te volgen.
* Gaschromatografie: Scheidt en identificeert verschillende componenten van een mengsel, zodat u de vorming of verdwijning van specifieke verbindingen kunt volgen.
* titratie: Een techniek die wordt gebruikt om de concentratie van een stof te bepalen door deze te reageren met een oplossing van bekende concentratie. Het eindpunt van de titratie geeft de voltooiing van de reactie aan.
4. Equilibrium bereiken:
* Veel reacties gaan niet tot voltooiing, maar bereiken een staat van evenwicht waar de voorwaartse en omgekeerde reacties met dezelfde snelheid optreden. Dit betekent dat zowel reactanten als producten aanwezig zijn in een stabiel mengsel. Het bepalen van het evenwicht kan complex zijn en vereist vaak gespecialiseerde kennis en technieken.
Belangrijke overwegingen:
* reactiesnelheid: Sommige reacties gebeuren snel, terwijl anderen traag zijn. Het is cruciaal om de reactiesnelheid te begrijpen om te bepalen hoe lang het duurt voordat de reactie wordt voltooid.
* omkeerbaarheid: Sommige reacties zijn omkeerbaar, wat betekent dat de producten kunnen reageren om opnieuw de reactanten te vormen. Het is essentieel om omkeerbaarheid te overwegen bij het bepalen of een reactie echt is afgelopen.
Samenvattend is er geen enkele, universeel toepasbare methode om te weten wanneer een chemische reactie is beëindigd. U moet de specifieke reactie overwegen en de juiste technieken kiezen op basis van de beschikbare informatie en bronnen.
 Niet te laat om op hol geslagen klimaatverandering te voorkomen:EU
Niet te laat om op hol geslagen klimaatverandering te voorkomen:EU Insecten in gematigde loofbossen
Insecten in gematigde loofbossen Wat geloofde wetenschapper waar het waar was over de natuur?
Wat geloofde wetenschapper waar het waar was over de natuur?  Kunnen tandpastatubes in de VS worden gerecycled? Het komt dichterbij
Kunnen tandpastatubes in de VS worden gerecycled? Het komt dichterbij  Na overstromingen komen (weer) droogte. Betere indicatoren helpen ons te reageren
Na overstromingen komen (weer) droogte. Betere indicatoren helpen ons te reageren
Hoofdlijnen
- Gaat de celdeling alleen voor bij vrouwen?
- Wat kan in het echte leven worden vergeleken met de nucleolus?
- Een vis, twee vissen - met behulp van een nieuw door MBARI ontworpen camerasysteem om roodbaars te tellen
- Hoe heeft Robert Hooke bijgedragen aan de celtheorie?
- Wat zaagvissen werkelijk doen met hun zaag
- Waarom worden cellen de basiseenheid van het leven genoemd?
- Van groeiende wortels tot aanwijzingen over hoe stamcellen hun lot bepalen
- Papegaaien geven de voorkeur aan live videogesprekken boven het bekijken van vooraf opgenomen video's van andere vogels
- Tegelijkertijd inzoomen door tijd en ruimte met superresolutie om te begrijpen hoe cellen zich delen
- Softwareprogramma Allchemy identificeert prebiotische synthese van biochemische verbindingen uit oer-precursoren

- Wetenschappers werken aan biologisch afbreekbaar plastic van zonlicht

- Goedkopere waterstofproductie

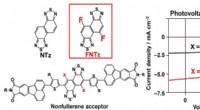
- Beheersing van openingen in de organische halfgeleiderband door fluorering van elektronenacceptor
- Onderzoekers ontwikkelen hulpmiddel om te helpen bij ontwikkeling, efficiëntie van auto's op waterstof

 Bergkristallen uit de diepte geven microscopische aanwijzingen voor grondbewegingen bij aardbevingen
Bergkristallen uit de diepte geven microscopische aanwijzingen voor grondbewegingen bij aardbevingen Bioactieve glas nanovezels geproduceerd
Bioactieve glas nanovezels geproduceerd Wat is werk in de fysieke wetenschap?
Wat is werk in de fysieke wetenschap?  Onderzoekers ontwikkelen nieuwe paden voor zelf-geassembleerde nanostructuren
Onderzoekers ontwikkelen nieuwe paden voor zelf-geassembleerde nanostructuren Welk enzym voegt nucleïnezuren toe aan de DNA-keten?
Welk enzym voegt nucleïnezuren toe aan de DNA-keten?  Wat is de dichtheid van een pingpongbal?
Wat is de dichtheid van een pingpongbal?  Welke 3 dingen laten celdeling levende organismen toe?
Welke 3 dingen laten celdeling levende organismen toe?  Hoe ziet een ringvormige zonsverduistering eruit?
Hoe ziet een ringvormige zonsverduistering eruit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

