
Wetenschap
Wat was de definitie van een atoom?
Vroege definities:
* oude Griekse filosofen (Democritus, Leucippus): Het idee van een atoom kwam voor het eerst naar voren in het oude Griekenland. Ze stelden atomen voor als ondeelbare, vaste deeltjes die alle materie vormden.
* John Dalton (1808): De atomaire theorie van Dalton bood een meer wetenschappelijke basis voor het atoom:
* Elementen zijn samengesteld uit atomen.
* Alle atomen van een bepaald element zijn identiek.
* Atomen van verschillende elementen hebben verschillende massa's.
* Atomen kunnen niet worden gemaakt of vernietigd, alleen herschikt.
Moderne definities:
* J.J. Thomson (1897): Thomson's ontdekking van het elektron leidde tot het pruimpuddingmodel, waarbij een positief geladen bol negatief geladen elektronen bevatte ingebed.
* Ernest Rutherford (1911): Rutherford's Gold Foil -experiment toonde aan dat het atoom een dichte, positief geladen kern heeft omringd door een meestal lege ruimte die elektronen bevat.
* Niels Bohr (1913): Bohr stelde voor dat elektronen specifieke energieniveaus rond de kern bezetten en de emissie van licht uit atomen verklaren.
* kwantummechanica: In het begin van de 20e eeuw bracht de kwantummechanica een revolutie teweeg in het begrip van het atoom. Het onthulde dat elektronen zich gedragen als zowel golven als deeltjes, en hun gedrag wordt bepaald door waarschijnlijkheden in plaats van vaste banen.
Huidige definitie:
Tegenwoordig wordt het atoom gedefinieerd als de kleinste eenheid van een element dat de chemische eigenschappen van dat element behoudt. Het bestaat uit een nucleus Bevat protonen en neutronen, en een omliggende wolk van elektronen .
Hier is een belangrijke afhaalmaaltijd:
* Een atoom is geen kleine, solide bol. Het is een complex systeem met een centrale kern omgeven door een probabilistische wolk van elektronen.
Opmerking: De definitie van een atoom evolueert nog steeds naarmate wetenschappers de aard van materie op steeds kleinere schalen blijven verkennen.
 Chemici leiden de juiste structuur af van de A- en B-baulamycinen
Chemici leiden de juiste structuur af van de A- en B-baulamycinen Waarom zijn zuurstof en silicium de meest voorkomende elementen gevonden in mineralen?
Waarom zijn zuurstof en silicium de meest voorkomende elementen gevonden in mineralen?  Nieuwe methode voor het produceren van optische materialen verlaagt de kosten, verbetert de prestaties
Nieuwe methode voor het produceren van optische materialen verlaagt de kosten, verbetert de prestaties Wat is de massa van 3,09x1024 atomen zwavel in gram?
Wat is de massa van 3,09x1024 atomen zwavel in gram?  Een suikeroplossing van 20% maken
Een suikeroplossing van 20% maken
 Kan genderdiversiteit in raden van bestuur de sociale betrokkenheid en duurzaamheid van bedrijven verbeteren?
Kan genderdiversiteit in raden van bestuur de sociale betrokkenheid en duurzaamheid van bedrijven verbeteren?  Is het door de wind geblazen slib dat het landschap deken?
Is het door de wind geblazen slib dat het landschap deken?  Ideeën voor Science Fair-projecten over vis
Ideeën voor Science Fair-projecten over vis  Hoe u objecten waarneemt, wordt bepaald door welke dingen?
Hoe u objecten waarneemt, wordt bepaald door welke dingen?  Luchtvaartindustrie onder druk vanwege klimaatverandering
Luchtvaartindustrie onder druk vanwege klimaatverandering
Hoofdlijnen
- Hoe verschilt veldstudie van laboratoriumstudie?
- Hoe wetenschappers DNA-codes herontwerpen
- Wat betekent generiek?
- Wat voor soort relatie ontstaat er als een bij bloemen vliegt om nectar te krijgen?
- Waarom gebruiken microbiologen vlekken op cellen?
- Hoe planten suiker gebruiken om wortels te produceren
- Reproductie waar is er maar één ouder?
- Hoe wordt het overervingspatter tussen ouders en nakomelingen diagrammatisch weergegeven?
- Wat zijn de eerste stappen die wetenschappers nemen om de oorzaak van een ziekte te analyseren?
- Een betere beoordeling van de gevoeligheid van bacteriën voor antibiotica kan de manier waarop medicijnen worden voorgeschreven veranderen

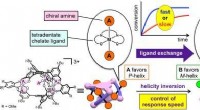
- Chiraliteitsinversie in een spiraalvormig molecuul bij gecontroleerde snelheden
- DNA-schade veroorzaakt door migrerende lichtenergie

- Gezien de impact van de chemiecocktail voor binnenshuis

- Het opruimen van Tsjernobyl kan worden geholpen door een nieuwe benadering voor röntgenanalyse

 Waarom beweegt een slang op glad oppervlak?
Waarom beweegt een slang op glad oppervlak?  Martian CSI onthult hoe asteroïde-inslagen stromend water creëerden onder de rode planeet
Martian CSI onthult hoe asteroïde-inslagen stromend water creëerden onder de rode planeet Meteorieten geven aanwijzingen voor de oorsprong van het zonnestelsel
Meteorieten geven aanwijzingen voor de oorsprong van het zonnestelsel Wat biedt een celergie?
Wat biedt een celergie?  Wat betekent axonaal?
Wat betekent axonaal?  Wat produceren sterren door fusie?
Wat produceren sterren door fusie?  Modellen combineren met experimenten om efficiëntere zonnecellen te bouwen
Modellen combineren met experimenten om efficiëntere zonnecellen te bouwen Wat is de transformatie van een bestaande rots vanwege hoge hitte en druk?
Wat is de transformatie van een bestaande rots vanwege hoge hitte en druk?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

