
Wetenschap
Wat is de Lewis Dot -structuur voor natriumhydroxide?
* ionische binding: Natriumhydroxide wordt gevormd door de elektrostatische aantrekkingskracht tussen een positief geladen natriumion (Na+) en een negatief geladen hydroxide-ion (OH-).
* elektronenoverdracht: Natrium verliest zijn valentie-elektron om een kation te worden (Na+), terwijl zuurstof in het hydroxide-ion een elektron wint om een stabiel octet te bereiken, waardoor een negatief geladen hydroxide-ion (OH-) wordt gevormd.
Daarom vertegenwoordigen we in plaats van een Lewis DOT -structuur de structuur van NaOH als:
* formule: Nao
* ionische structuur: Na+ oh-
Verklaring:
* Natriumion (Na+): Het natriumion heeft zijn enkele valentie -elektron verloren en heeft een +1 lading. Het wordt weergegeven als eenvoudig Na+.
* Hydroxide-ion (OH-): Het hydroxide -ion heeft een elektron gewonnen en vormt een covalente binding tussen zuurstof en waterstof. Zuurstof heeft 6 valentie -elektronen en het toegevoegde elektron zorgt ervoor dat het 7. Waterstof heeft 1 elektron en de binding gebruikt 2 elektronen. Dit laat 6 elektronen rond zuurstof, die wordt weergegeven als 3 eenzame paren, waardoor het hydroxide -ion A -1 lading krijgt.
Belangrijke opmerking: Hoewel we geen traditionele Lewis Dot -structuur kunnen tekenen, kunnen we de afzonderlijke ionen afzonderlijk weergeven, met de overdracht van elektronen en de resulterende ladingen.
 Energieopslagmaterialen opgebouwd uit moleculaire blokken van nanoformaat
Energieopslagmaterialen opgebouwd uit moleculaire blokken van nanoformaat Hoe ijs werkt
Hoe ijs werkt  Wat gebeurt er als deeltjes in een vloeistof worden afgekoeld?
Wat gebeurt er als deeltjes in een vloeistof worden afgekoeld?  Wat is de formule voor ionische verbinding Al 3 en S2-?
Wat is de formule voor ionische verbinding Al 3 en S2-?  Ingenieurs pionieren met het vormingsproces van platinagranaten, eerste waarneming ooit bereiken
Ingenieurs pionieren met het vormingsproces van platinagranaten, eerste waarneming ooit bereiken
Hoofdlijnen
- De vorm van het leven:onderzoek werpt licht op hoe cellen nemen
- Voorbeelden van diffusie in organen
- Welk gedrag zou sommige evolutionaire psychologen bieden als bewijs van hun theorie?
- Welke vorm van gen die altijd zelfs in de aanwezigheid recessief allel toont?
- Welke witte bloedcellen produceren antilichamen en spelen een rol bij de immuunrespons?
- Welke van de volgende is geen divisie-niet-zaadplanten?
- Hoe worden wetenschappelijke schaar genoemd?
- Wat is de wetenschappelijke methode een proces van?
- Hoe is de uiterlijke verschijning van een eigenschap?
- Organische polymere scintillatoren prikkelen de röntgengemeenschap

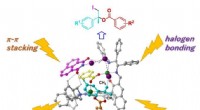
- Asymmetrische joodverestering van eenvoudige alkenen door concerto-katalysator
- Nieuwe elektroden kunnen de efficiëntie van elektrische voertuigen en vliegtuigen verhogen

- 'S Werelds eerste biobricks gekweekt uit menselijke urine

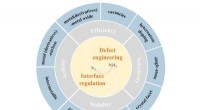
- Defect- en interface-engineering voor e-NRR onder omgevingsomstandigheden
 Niet-menselijk leven moet centraal staan bij het oplossen van duurzaamheidsproblemen
Niet-menselijk leven moet centraal staan bij het oplossen van duurzaamheidsproblemen In welke landen zijn fossiele brandstoffen gevonden?
In welke landen zijn fossiele brandstoffen gevonden?  Bestaat de aarde uit verschillende lagen?
Bestaat de aarde uit verschillende lagen?  Wat bepaalt het aantal halve golfsghts dat in lengtekering past?
Wat bepaalt het aantal halve golfsghts dat in lengtekering past?  Wat is het resultaat van afbuiging geladen deeltjes langs Van Allen -riemen?
Wat is het resultaat van afbuiging geladen deeltjes langs Van Allen -riemen?  Een verklaring over de zon van deel A is de corona -heter dan fotosfeer Welke van de volgende verklaringen biedt observationeel bewijs voor deze claim?
Een verklaring over de zon van deel A is de corona -heter dan fotosfeer Welke van de volgende verklaringen biedt observationeel bewijs voor deze claim?  Wat is de zwaartekracht op een object?
Wat is de zwaartekracht op een object?  Zijn andere tegenstrijdigheden in de wet van natuurbeschermingsenergie in de gebiedswetenschappen?
Zijn andere tegenstrijdigheden in de wet van natuurbeschermingsenergie in de gebiedswetenschappen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

