
Wetenschap
Wat is de evenwichtige vergelijking voor verbranding van C3H6O?
2 C3H6O + 9 O2 → 6 CO2 + 6 H2O
Hier is hoe je het in evenwicht kunt brengen:
1. Identificeer de reactanten en producten:
* reactanten: Propanal (C3H6O) en zuurstof (O2)
* Producten: Koolstofdioxide (CO2) en water (H2O)
2. Begin met het balanceren van de koolstofatomen: Er zijn 3 koolstofatomen aan de linkerkant en 1 rechts. Voeg een coëfficiënt van 3 toe voor CO2.
* 2 C3H6O + 9 O2 → 6 CO2 + 6 H2O
3. Breng de waterstofatomen in evenwicht: Er zijn 12 waterstofatomen aan de linkerkant en 12 aan de rechterkant, dus ze zijn al in balans.
4. Breng de zuurstofatomen in evenwicht: Er zijn 18 zuurstofatomen aan de linkerkant en 18 rechts. De vergelijking is nu in evenwicht.
Deze evenwichtige vergelijking toont aan dat 2 mol propanaal reageert met 9 mol zuurstof om 6 mol kooldioxide en 6 mol water te produceren.
 Hoe converteer je 1 ton CO2 naar kubieke voet?
Hoe converteer je 1 ton CO2 naar kubieke voet?  Wat als Titan Dragonfly een fusiemotor had?
Wat als Titan Dragonfly een fusiemotor had?  Waarom kun je wel de verschillende delen van een mechanisch mengsel zien, maar niet de oplossing?
Waarom kun je wel de verschillende delen van een mechanisch mengsel zien, maar niet de oplossing?  Wat is de chemische vergelijking die het proces van fotosynthese regelt?
Wat is de chemische vergelijking die het proces van fotosynthese regelt?  Wat is de vergelijking voor het produceren van ethylpropanoaat uit joodethaan?
Wat is de vergelijking voor het produceren van ethylpropanoaat uit joodethaan?
 Wat is Wild Life. Schrijf een korte opmerking over dieren in het wild?
Wat is Wild Life. Schrijf een korte opmerking over dieren in het wild?  Hoe Black Birds weg te houden van Bird Feeders
Hoe Black Birds weg te houden van Bird Feeders Hoe een Trump-grensmuur de natuur zou beïnvloeden?
Hoe een Trump-grensmuur de natuur zou beïnvloeden?  De overstromingsfrequentie van 's werelds grootste rivier is vervijfvoudigd
De overstromingsfrequentie van 's werelds grootste rivier is vervijfvoudigd NASA-NOAA-satelliet vangt tropische cycloon Blake en branden in West-Australië
NASA-NOAA-satelliet vangt tropische cycloon Blake en branden in West-Australië
Hoofdlijnen
- Hoe beïnvloeden Genotype en Fenotype hoe je eruit ziet?
- Waarom leven dieren in de Dode Zee?
- Steunt dendrieten het axon van binnenuit?
- Geven mensen overal minder om hun katten dan om honden?
- Evolutie hoe werkt
- Hoe werkt ureum denaturisch?
- Wie is er bekend om ontdekkingen in radioactiviteit?
- Waarom GNEP niet naar de toekomst kan springen
- Hoe boomkikker-embryo's met rode ogen binnen enkele seconden uitkomen (Update)
- Strategieën om grotere poriën te genereren in metaal-organische raamwerken
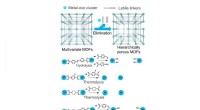
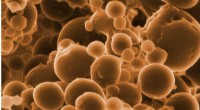
- Kenniskloof gedicht in ons begrip van degradatie van ethaan
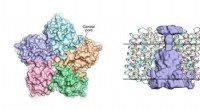
- Wetenschappers onthullen de structuur van virale rodopsines
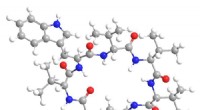
- Natuurlijke antibiotica multi-level aanvalsstrategie voorkomt resistentie
- Welke dranken barsten van het umami-potentieel?

 DNA-modificatie belangrijk voor het tot zwijgen brengen van endogene retrovirussen
DNA-modificatie belangrijk voor het tot zwijgen brengen van endogene retrovirussen Bestrijding van de klimaatverandering:waarom beleggers hun aandelen in fossielebrandstofbedrijven moeten behouden
Bestrijding van de klimaatverandering:waarom beleggers hun aandelen in fossielebrandstofbedrijven moeten behouden  Hoe maak je gebruik van elastische energie?
Hoe maak je gebruik van elastische energie?  Welke heeft de langere golflengte -infrarood of X Ray?
Welke heeft de langere golflengte -infrarood of X Ray?  Welke stad is 35 graden North Latitude en 43 West Loogte?
Welke stad is 35 graden North Latitude en 43 West Loogte?  Hoe een elektromagneet te maken
Hoe een elektromagneet te maken  Vooruitgang en uitdagingen bij het begrijpen van samengestelde weers- en klimaatextremen
Vooruitgang en uitdagingen bij het begrijpen van samengestelde weers- en klimaatextremen  Hoe kan Illinois het probleem van PFAS-vervuiling aanpakken?
Hoe kan Illinois het probleem van PFAS-vervuiling aanpakken?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

