
Wetenschap
Wat is de elektronische structuur van een chloride -ion?
1. Startpunt:chloor atom
* Chloor (CL) heeft een atoomnummer van 17, wat betekent dat het 17 protonen en 17 elektronen heeft.
* De elektronische configuratie is:1S² 2S² 2P⁶ 3S² 3P⁵
2. Vorming van het chloride -ion
* Chloor krijgt één elektron om een stabiel octet (8 elektronen) in zijn buitenste schaal te bereiken.
* Dit creëert een negatieve lading, wat resulteert in het chloride -ion (CL⁻).
3. Elektronische configuratie van chloride -ion
* De elektronische configuratie van het chloride -ion wordt:1S² 2S² 2P⁶ 3S² 3P⁶
Vereenvoudigde weergave:
* Het chloride -ion heeft een volledige buitenste schaal met 8 elektronen (2 in de 3s orbital en 6 in de 3P -orbitalen).
* Dit geeft het een stabiele, edelgasconfiguratie vergelijkbaar met Argon (AR).
Sleutelpunten:
* Het chloride -ion is negatief geladen omdat het één elektron heeft gekregen.
* De elektronische configuratie is hetzelfde als Argon, waardoor het zeer stabiel is.
* Deze stabiliteit is de reden waarom chloride -ionen gebruikelijk zijn in ionische verbindingen.
 Kunstmatig rif maakt zijn debuut in Sydney Opera House
Kunstmatig rif maakt zijn debuut in Sydney Opera House Watergebruik in de landbouw in de VS neemt af voor de meeste gewassen en veeteelt
Watergebruik in de landbouw in de VS neemt af voor de meeste gewassen en veeteelt De omgeving biedt twee soorten natuurlijke hulpbronnen- kapitaalbronnen en mensen zijn?
De omgeving biedt twee soorten natuurlijke hulpbronnen- kapitaalbronnen en mensen zijn?  Welke dieren eten eendenkroos?
Welke dieren eten eendenkroos?  Van bladeren tot wolken - onthullen hoe de uitstoot van bomen de lucht om ons heen vormt
Van bladeren tot wolken - onthullen hoe de uitstoot van bomen de lucht om ons heen vormt
Hoofdlijnen
- UITLEG:Wat maakt zangvogels uit het midden van de Atlantische Oceaan ziek?
- De belangrijkste werking van de flexor hallicus longus spier is om?
- Wat is een zaadje in de biologie?
- Chromosomen bevestigd aan de spindelvezels door onverdeelde structuren wordt wat genoemd?
- Kan B genotype trouwen met een a en o negatief produceren?
- Kan alle micro -organisme worden gekweekt met behulp van synthetische media?
- Wat is de overtuiging dat Charles -theorieën zoals het overleven van Fittest van toepassing zijn op menselijke groepen en rassen?
- Microbiële ziekten en mutaties: wat is het ?, Lijsten & Oorzaken
- Duitsland zegt dat massale vissterfte in de rivier de Oder een door de mens veroorzaakte ramp is
- Verbindingen in een Aziatische gefermenteerde vispasta kunnen een hoog cholesterolgehalte verlagen

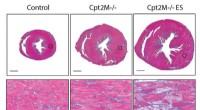
- Onderzoek toont aan dat vette brandstof nodig is om cardiale hypertrofie om te keren
- Draagbaar apparaat verlicht de weg naar betere detectie van door voedsel overgedragen ziekten

- Het produceren van foutloze metaalkristallen van ongekende grootte

- Terminator-achtig vloeibaar metaal beweegt en rekt zich uit in de 3D-ruimte

 Top 5 gekke overheidsexperimenten
Top 5 gekke overheidsexperimenten  Grafeen wordt helder:'s werelds dunste gloeilamp ontwikkeld
Grafeen wordt helder:'s werelds dunste gloeilamp ontwikkeld Welke oceaan heeft veel kleine verspreide eilanden die zijn gevormd uit de uiteinden van uitgestorven vulkanen?
Welke oceaan heeft veel kleine verspreide eilanden die zijn gevormd uit de uiteinden van uitgestorven vulkanen?  Amazon blokkeert Australië van wereldwijde sites vanwege belasting
Amazon blokkeert Australië van wereldwijde sites vanwege belasting Musk hoopt dat Mechazilla de Starship- en Super Heavy-boosters zal vangen en monteren voor snel hergebruik
Musk hoopt dat Mechazilla de Starship- en Super Heavy-boosters zal vangen en monteren voor snel hergebruik De druk staat nu op Facebook om politieke advertenties te verbieden, te
De druk staat nu op Facebook om politieke advertenties te verbieden, te Waarom willen we krassen?
Waarom willen we krassen?  Hoe werkt een katrolsysteem?
Hoe werkt een katrolsysteem?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

