
Wetenschap
Welke atomen zijn het meest reactief?
* zeer elektronegatief: Deze atomen hebben een sterke aantrekkingskracht op elektronen, waardoor ze graag elektronen willen krijgen en bindingen vormen. Voorbeelden zijn fluor (F) en zuurstof (O).
* Heb een enkel ongepaard elektron in hun buitenste schaal: Hierdoor reageren ze zeer waarschijnlijk met andere atomen om hun buitenste schaal te voltooien en stabiliteit te bereiken. Voorbeelden zijn waterstof (H) en de halogenen (F, CL, BR, I).
* hebben een lage ionisatie -energie: Deze atomen verliezen gemakkelijk elektronen en worden kationen. Voorbeelden zijn alkali -metalen (LI, NA, K, RB, CS).
Hier is een uitsplitsing van de meest reactieve elementen en hun kenmerken:
* Groep 1 (Alkali metalen): Deze elementen hebben slechts één valentie -elektron, waardoor ze zeer reactief zijn. Ze verliezen dit elektron gemakkelijk om positieve ionen (kationen) te vormen en reageren gemakkelijk met water en andere elementen.
* Groep 2 (Alkaline Earth Metals): Deze elementen hebben twee valentie -elektronen en zijn minder reactief dan alkali -metalen, maar nog steeds zeer reactief. Ze vormen positieve ionen en reageren met water, hoewel meestal niet zo krachtig als alkali -metalen.
* Groep 17 (halogenen): Deze elementen hebben zeven valentie -elektronen en hebben er nog een nodig om hun buitenste schaal te voltooien. Ze zijn zeer reactief en krijgen gemakkelijk een elektron om negatieve ionen (anionen) te vormen.
* Groep 18 (edelgassen): Deze elementen hebben een volledige buitenste schaal van elektronen, waardoor ze zeer stabiel en niet -reactief zijn. Ze worden zelden gevonden in verbindingen.
In het algemeen neemt de reactiviteit toe van rechts naar links en van boven naar beneden op de periodieke tabel. Dit komt omdat elementen aan de linkerkant minder valentie -elektronen hebben en ze gemakkelijker verliezen, terwijl elementen aan de bovenkant minder elektronenschalen hebben, waardoor ze gemakkelijker worden om elektronen te krijgen of te verliezen.
Houd er rekening mee: Reactiviteit is een complex concept dat kan worden beïnvloed door verschillende factoren. Hoewel het bovenstaande een algemeen overzicht biedt, kunnen specifieke reacties en de reactiviteit van individuele elementen sterk variëren.
 Waar is het grootste deel van de massa van een atoom gelegen?
Waar is het grootste deel van de massa van een atoom gelegen?  Nieuwe methode zet methaan in aardgas bij kamertemperatuur om in methanol
Nieuwe methode zet methaan in aardgas bij kamertemperatuur om in methanol Welk organisch molecuul regelt de reactiesnelheden en reguleert celprocessen?
Welk organisch molecuul regelt de reactiesnelheden en reguleert celprocessen?  Wat is een eiwitmolecuul dat werkt als biologische katalysator om chemische reacties te versnellen door de energie van activering te verlagen?
Wat is een eiwitmolecuul dat werkt als biologische katalysator om chemische reacties te versnellen door de energie van activering te verlagen?  Wat is de dichtheid van fenol -formaldehydehars?
Wat is de dichtheid van fenol -formaldehydehars?
 Waterinfrastructuur ontwerpen voor klimaatonzekerheid
Waterinfrastructuur ontwerpen voor klimaatonzekerheid Oude plankton-achtige microfossielen strekken zich uit over twee continenten
Oude plankton-achtige microfossielen strekken zich uit over twee continenten Kan klimaatverandering de Golfstroom stilleggen?
Kan klimaatverandering de Golfstroom stilleggen? Nauwkeurigheid van regenvoorspelling onderzoeken met betrekking tot extreme regenval in de provincie Henan, China
Nauwkeurigheid van regenvoorspelling onderzoeken met betrekking tot extreme regenval in de provincie Henan, China Wat zijn natuurlijke hulpbronnen?
Wat zijn natuurlijke hulpbronnen?
Hoofdlijnen
- Hoe wordt het genoemd als een cytoplasma begint te scheiden?
- Acute tastzin helpt kolibries dichtbij een bloem te zweven zonder er tegenaan te botsen, blijkt uit onderzoek
- Welk type cellen bevatten een kern?
- In plantencellen wordt de splitsing van cel in 2 veroorzaakt door wat?
- Waarom koningsbavianenspinnengif zo pijnlijk is
- Virtual reality voor bacteriën
- Wat is het verschil tussen een levend en niet-levend organisme?
- Wat maakt een systeembenadering geldig voor wetenschappelijk onderzoek?
- Welk enzym is verantwoordelijk voor het decoderen van de DNA -streng in een mRNA?
- Studie doet twijfel rijzen over de nauwkeurigheid van mobiele apparaten voor het testen van medicijnen

- Duidelijk, geleidende coating kan geavanceerde zonnecellen beschermen, aanraakschermen

- MOF-cokatalysator maakt selectiviteit van vertakte aldehyden tot 90% mogelijk

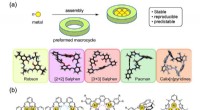
- Metaalcomplexen gemaakt van cyclische moleculen
- Een beter microgrid printen

 De noordpool ligt ten noorden van welk eiland?
De noordpool ligt ten noorden van welk eiland?  Lanthanide-nanodeeltjes maken continue-golf NIR STED-microscopie mogelijk
Lanthanide-nanodeeltjes maken continue-golf NIR STED-microscopie mogelijk Kun jij echt een brand ontlopen?
Kun jij echt een brand ontlopen?  Rechters behandelen antitrustzaak over verkoop iPhone-apps
Rechters behandelen antitrustzaak over verkoop iPhone-apps Welke kleur heeft de zon eigenlijk?
Welke kleur heeft de zon eigenlijk?  Bescheiden biologen als virussen als leven of niet -leven?
Bescheiden biologen als virussen als leven of niet -leven?  Hoe verhoogt de ontlading de erosie op het aardoppervlak?
Hoe verhoogt de ontlading de erosie op het aardoppervlak?  Heeft de zon een duister geheim?
Heeft de zon een duister geheim?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

