
Wetenschap
Is het smeltpunt van broom hoger of lager dan chloor?
Dit is waarom:
* intermoleculaire krachten: Bromine (Br₂) en chloor (CL₂) zijn beide diatomaire halogenen. Ze ervaren van der Waals -troepen, met name de dispersiekrachten in Londen. Deze krachten komen voort uit tijdelijke schommelingen in elektronenverdeling, waardoor tijdelijke dipolen ontstaan.
* Grootte en polariseerbaarheid: Broomatomen zijn groter dan chlooratomen. Grotere atomen hebben een grotere elektronenwolk, waardoor ze meer polariseerbaar zijn. Dit betekent dat tijdelijke dipolen sterker en gemakkelijker te vormen zijn in broom in vergelijking met chloor.
* Sterkere intermoleculaire krachten: Sterkere dispersiekrachten in Londen in broom resulteren in een hoger smeltpunt omdat meer energie nodig is om deze krachten te overwinnen en de intermoleculaire bindingen te doorbreken.
smeltpunten:
* Chloor (CL₂):-101,5 ° C
* Bromine (Br₂):-7.2 ° C
 Verf met een ingrediënt dat voorkomt dat scheiding wordt genoemd wat in de wetenschap?
Verf met een ingrediënt dat voorkomt dat scheiding wordt genoemd wat in de wetenschap?  Wat is de som van de coëfficiënten SF4 plus H20 H2sSO HF?
Wat is de som van de coëfficiënten SF4 plus H20 H2sSO HF?  Het element dat 3 elektronen in het neutrale atoom bevat, is?
Het element dat 3 elektronen in het neutrale atoom bevat, is?  Wat is de hardheid van peridot in Mohs-hardheidsschaal?
Wat is de hardheid van peridot in Mohs-hardheidsschaal?  Wat is de chemische vergelijking voor reacties wanneer koper wordt toegevoegd aan aluminiumsulfaat?
Wat is de chemische vergelijking voor reacties wanneer koper wordt toegevoegd aan aluminiumsulfaat?
Hoofdlijnen
- Giftige mannelijkheid:waarom mannelijke trechterwebspinnen zo gevaarlijk zijn
- Wat is het genotype van twee zwarte heterozygote cavia?
- Verplaats fagocytose stoffen uit een cel?
- De delen van een gistcel
- UV-licht: positieve en negatieve effecten
- Wat is de wetenschap in het Latijn?
- Wat eet Earwig?
- Wat is een organel in een cel?
- Wat is het huidige zeven stappensysteem om alle levende organismen te classificeren?
- Ontwikkeling van vereenvoudigde nieuwe massaspectrometrische techniek met behulp van laser en grafeen

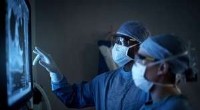
- Kleurveranderingstest om kankeronderzoek vooruit te helpen
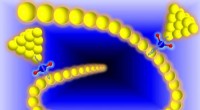
- Onderzoekers creëerden een klein circuit door een enkel watermolecuul
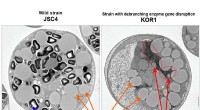
- Koolhydraten omzetten in lipiden voor biobrandstoffen voor microalgen
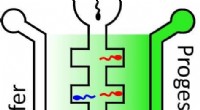
- Een nieuwe manier om mannelijke vruchtbaarheid te beoordelen
 Bergerosie kan CO2 aan de atmosfeer toevoegen
Bergerosie kan CO2 aan de atmosfeer toevoegen Kan carbonzuur reageren met Grignard-reagens?
Kan carbonzuur reageren met Grignard-reagens?  Hoe vind je de molaire massa van berylliumoxide?
Hoe vind je de molaire massa van berylliumoxide?  Wetenschappers vinden een effectieve manier om brandstof voor waterstofmotoren te verkrijgen
Wetenschappers vinden een effectieve manier om brandstof voor waterstofmotoren te verkrijgen Wat is het lot van ei- en endosperm -kern in dubbele bemestingsinstallatie?
Wat is het lot van ei- en endosperm -kern in dubbele bemestingsinstallatie?  Hoe te gedijen in accuzuur en tussen giftige metalen
Hoe te gedijen in accuzuur en tussen giftige metalen  Een filament dat geschikt is voor de ruimte - het is bewezen dat zijde gedijt bij temperaturen in de ruimte
Een filament dat geschikt is voor de ruimte - het is bewezen dat zijde gedijt bij temperaturen in de ruimte Wat maakt de vulkaan kilauea beroemd?
Wat maakt de vulkaan kilauea beroemd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

