
Wetenschap
Wat leidt elektriciteit wanneer oplost in water?
Dit is waarom:
* elektrolyten zijn stoffen die ionen (geladen deeltjes) bevatten wanneer opgelost in water.
* ionen zijn atomen of moleculen die elektronen hebben gewonnen of verloren, waardoor ze een positieve of negatieve lading hebben.
* Water is een polair molecuul, wat betekent dat het een positief en negatief einde heeft. Hierdoor kan het ionen aantrekken en omringen, waardoor ze van elkaar worden gebroken.
* Wanneer deze vrije ionen aanwezig zijn in een oplossing, kunnen ze vrij bewegen en een elektrische stroom dragen.
Voorbeelden van elektrolyten:
* zouten: NaCl (tafelzout) lost op in Na+ en clies.
* zuren: HCL (zoutzuur) lost op in H+ en clionen.
* Bases: NaOH (natriumhydroxide) lost op in Na+ en OH-ionen.
Niet-elektrolyten:
* stoffen die geen ionen bevatten wanneer opgelost in water geen elektriciteit leiden. Voorbeelden zijn suiker (sucrose) en alcohol (ethanol).
Hoofdlijnen
- Wetenschappelijke evaluatie van neushoorndiëten verbetert dierentuin
- Hoe de lengte van DNA-fragmenten te berekenen
- Wat biedt informatie voor celgroei en -functie?
- Wat zijn staafvormige structuren gevonden in een kern?
- Waarom zijn orchideeën zo succesvol?
- Wat is de naam van organel die betrokken is bij zuurstof die proces vereist door welke energie -macromoleculen ATP heeft opgeslagen?
- Welke psycholoog zei nog dat wat we bereiken te wijten is aan de samenstelling van onze genen?
- Een evolutiepatroon waarin iets verschillende soorten evolueren van één gemeenschappelijke voorouder?
- Welke moleculen behouden de vorm die nodig is om biologisch actief te zijn vanwege intermoleculaire krachten?
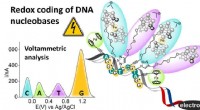
- Nieuwe methode voor het labelen van DNA-basen voor sequencing
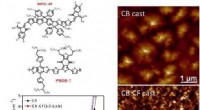
- Binair oplosmiddelmengsel dat het hoge rendement van polymere zonnecellen verhoogt
- Onderzoekers ontwikkelen een nieuwe manier om een spectrum van natuurlijk ogende haarkleuren te creëren

- Kankercellen kunnen over langere afstanden in het lichaam communiceren

- Leven bevroren in de tijd onder een elektronenmicroscoop krijgt Nobelprijs
 Wat is koolstofreductie?
Wat is koolstofreductie?  Voorbereidingen voltooid in West-Australië voor de bouw van de grootste telescoop ter wereld
Voorbereidingen voltooid in West-Australië voor de bouw van de grootste telescoop ter wereld Voor een bijzondere Valentijn? Beyond diamanten en edelstenen:'s werelds zeldzaamste mineralen
Voor een bijzondere Valentijn? Beyond diamanten en edelstenen:'s werelds zeldzaamste mineralen  Basismaterialen gebruikt in een elektrische generator
Basismaterialen gebruikt in een elektrische generator NASA's Webb Telescope General Observer wetenschappelijke programma's geselecteerd
NASA's Webb Telescope General Observer wetenschappelijke programma's geselecteerd De dodelijkste vulkaanuitbarstingen van de afgelopen 25 jaar
De dodelijkste vulkaanuitbarstingen van de afgelopen 25 jaar Colombia verbiedt sportjacht
Colombia verbiedt sportjacht Hoe bereken je de hoeveelheid mechanische energie in een object?
Hoe bereken je de hoeveelheid mechanische energie in een object?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


