
Wetenschap
Waarom is watermolecuul polair?
1. ongelijke delen van elektronen (polaire covalente bindingen): Het zuurstofatoom in water is meer elektronegatief dan de waterstofatomen. Dit betekent dat zuurstof de gedeelde elektronen in de covalente bindingen sterker aantrekt, waardoor een gedeeltelijke negatieve lading (A-) op het zuurstofatoom en gedeeltelijke positieve ladingen (A+) op de waterstofatomen ontstaat.
2. gebogen moleculaire geometrie: Het watermolecuul heeft een gebogen of V-vormige geometrie vanwege de aanwezigheid van twee eenzame paren elektronen op het zuurstofatoom. Deze vorm zorgt ervoor dat de gedeeltelijke positieve ladingen van de waterstofatomen zich aan één kant van het molecuul bevinden, en de gedeeltelijke negatieve lading van het zuurstofatoom ligt aan de andere kant, waardoor een dipoolmoment ontstaat.
3. resulterend dipoolmoment: De ongelijke verdeling van ladingen creëert een netto dipoolmoment, wat betekent dat het molecuul een positief en negatief einde heeft, waardoor het polair is. Dit dipoolmoment is verantwoordelijk voor veel van de unieke eigenschappen van water, zoals het hoge kookpunt, het vermogen om veel stoffen op te lossen en zijn rol als oplosmiddel in biologische systemen.
Samenvattend: De combinatie van polaire covalente bindingen en gebogen moleculaire geometrie resulteert in een ongelijke verdeling van ladingen in het watermolecuul, waardoor het een polair molecuul is.
 Waarom is het smeltpunt van arseen hoger dan het kookpunt?
Waarom is het smeltpunt van arseen hoger dan het kookpunt?  Nieuwe supramoleculaire copolymeren aangedreven door zelfsortering van moleculen
Nieuwe supramoleculaire copolymeren aangedreven door zelfsortering van moleculen Wat is iets interessants aan Titanium?
Wat is iets interessants aan Titanium?  Welke verbinding heeft 1 kaliumstikstof en 3
Welke verbinding heeft 1 kaliumstikstof en 3  Een vloeistof met een vaste vaste oplossing wordt oplossing genoemd, hoe kunt u terugkomen uit de oplossing?
Een vloeistof met een vaste vaste oplossing wordt oplossing genoemd, hoe kunt u terugkomen uit de oplossing?
 De studie van de aarde in al zijn variëteit?
De studie van de aarde in al zijn variëteit?  NASA-infraroodbeelden onthullen krachtige tropische cycloon Idai aan de kust van Mozambique
NASA-infraroodbeelden onthullen krachtige tropische cycloon Idai aan de kust van Mozambique Weersvoorspellingen die uitbraken van meningitis voorspellen
Weersvoorspellingen die uitbraken van meningitis voorspellen Technologie vanuit de lucht brengt nieuwe hoop om ondiepe watervoerende lagen in de meest dorre woestijnen van de aarde in kaart te brengen
Technologie vanuit de lucht brengt nieuwe hoop om ondiepe watervoerende lagen in de meest dorre woestijnen van de aarde in kaart te brengen  Hoe extratropische interacties tussen oceaan en atmosfeer kunnen bijdragen aan de variabiliteit van straalstromen
Hoe extratropische interacties tussen oceaan en atmosfeer kunnen bijdragen aan de variabiliteit van straalstromen
Hoofdlijnen
- Waarom bevatten niet alle plantencellen chloroplasten?
- Welke structuren in de groei en reproductie van de kern controleren celcellen?
- Intron: definitie, functie en belang bij RNA-splitsing
- Georganiseerd worden:onderzoek laat zien hoe borstcelgemeenschappen zich in weefsel organiseren
- Heeft de Noordpool Californië teisteren? Honderden trekkende zeevogels spoelen aan
- Morfogenese in planten is het gevolg van wat?
- Welke rol heeft NADPH in fotosynthese?
- Wat is de grootte van nucleus met massanummer 216?
- Hoeveel dierlijke cellen passen binnen één mm?
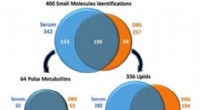
- Bij longitudinaal onderzoek gedroogde bloedvlekmonsters spelen een rol
- Hightech printen kan helpen om pijnlijke schoten te voorkomen

- Onderzoekers tonen rol voor cyanide bij ontstaan van leven

- Nieuwe slimme materialen kunnen een nieuw onderzoeksveld openen

- Synthetisch rubber presteert beter dan natuurlijk rubber

 Wat is dynamische prijsstelling? Een wetenschapper op het gebied van operations management legt uit
Wat is dynamische prijsstelling? Een wetenschapper op het gebied van operations management legt uit Wat zijn symbolen en waarom?
Wat zijn symbolen en waarom?  Wat voor soort weer gebeurt op Mars?
Wat voor soort weer gebeurt op Mars?  Hoe worden sommige metalen beschermd tegen chemische verandering?
Hoe worden sommige metalen beschermd tegen chemische verandering?  Als exoplaneten bliksem hebben, zal dat de zoektocht naar leven bemoeilijken
Als exoplaneten bliksem hebben, zal dat de zoektocht naar leven bemoeilijken  Grafieken met wetenschappelijke rekenmachines
Grafieken met wetenschappelijke rekenmachines Hoe diep zijn de oliebronnen in Golf van Mexico?
Hoe diep zijn de oliebronnen in Golf van Mexico?  Easy High School Physics Experiments
Easy High School Physics Experiments
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

