
Wetenschap
Hoe bedenk je molaire warmte van verbrandingsfenol bij 25 graden Celsius?
Waarom directe berekening niet mogelijk is:
* Complexe reactie: De verbranding van fenol (C6H5OH) is een complexe chemische reactie met meerdere stappen met de vorming van verschillende tussenproducten. Het direct toepassen van een eenvoudige formule is niet nauwkeurig.
* Standaardomstandigheden: Molaire verbrandingswarmte wordt meestal gerapporteerd onder standaardomstandigheden (298 K of 25 ° C en 1 atm druk). De standaardverbrandwarmte is echter niet direct van toepassing op alle temperaturen.
Hoe de molaire verbrandwatte te bepalen:
1. Experimentele meting: De meest nauwkeurige manier om de molaire verbrandingswarmte van fenol te bepalen, is door experimentele meting met behulp van een calorimeter. Dit omvat zorgvuldig het verbranden van een bekende massa fenol onder gecontroleerde omstandigheden en het meten van de vrijgegeven warmte.
2. Gebruik van standaardvormingsthalpies: U kunt de molaire verbrandwatte schatten met behulp van Hess's wet en standaard enthalpieën van formatie (ΔHF °) voor de reactanten en producten:
* Vergelijking:
C6H5OH (L) + 7 O2 (G) → 6 CO2 (G) + 3 H2O (L)
* Hess's Law:
ΔHCombustion =σ ΔHf ° (producten) - σ Δhf ° (reactanten)
* Zoek standaard van formatie -enthalpies op: U moet de standaard enthalpies van formatie vinden voor fenol, zuurstof, koolstofdioxide en water. Deze waarden worden meestal aangetroffen in thermodynamische tabellen.
* Bereken: Vervang de waarden in de wetvergelijking van Hess om de geschatte molaire verbrandingswarmte te krijgen.
Belangrijke overwegingen:
* Staat van materie: Zorg ervoor dat de vorming enthalpies die u gebruikt, overeenkomen met de juiste toestanden van materie (vloeibaar fenol, gasvormige zuurstof, enz.) Bij de gegeven temperatuur.
* Temperatuurafhankelijkheid: De molaire verbrandingswarmte zal enigszins variëren met de temperatuur. Hoewel de standaardwaarde een goede benadering is bij 25 ° C, is deze mogelijk niet perfect nauwkeurig voor andere temperaturen.
Voorbeeld (geschatte waarde):
Laten we zeggen dat u de volgende standaard enthalpies van formatie vindt (in kj/mol):
* ΔHf ° (C6H5OH (L)) =-165.0
* ΔHf ° (o2 (g)) =0,0
* ΔHf ° (CO2 (G)) =-393.5
* ΔHf ° (H2O (L)) =-285.8
Gebruik van de wet van Hess:
ΔHCombustion =[6 (-393.5) + 3 (-285.8)]-[-165.0 + 7 (0.0)]
=-3053,8 kJ/mol
Onthoud: Dit is een geschatte waarde. Experimentele metingen zijn meestal nauwkeuriger.
 Welke andere methode om een vloeistof van een vaste stof te scheiden heb je vandaag geleerd dan filtratie?
Welke andere methode om een vloeistof van een vaste stof te scheiden heb je vandaag geleerd dan filtratie?  Fotochrome bismutcomplexen zijn veelbelovend voor optische geheugenelementen
Fotochrome bismutcomplexen zijn veelbelovend voor optische geheugenelementen Hyper-CEST NMR-techniek onthult ontbrekende structuur van een nieuw containermolecuul
Hyper-CEST NMR-techniek onthult ontbrekende structuur van een nieuw containermolecuul Onderzoeksteam ontwikkelt polymeren die bacteriën kunnen doden
Onderzoeksteam ontwikkelt polymeren die bacteriën kunnen doden  Wetenschappers maken eetbaar servies voor eenmalig gebruik gemaakt van appels
Wetenschappers maken eetbaar servies voor eenmalig gebruik gemaakt van appels
 Welke geografische kenmerken van Europa hadden invloed op exploratie?
Welke geografische kenmerken van Europa hadden invloed op exploratie?  Wat is het ontstaan van kleur?
Wat is het ontstaan van kleur?  Brandweerlieden proberen te voorkomen dat de brand op het Griekse eiland het bos bereikt
Brandweerlieden proberen te voorkomen dat de brand op het Griekse eiland het bos bereikt Belangrijkste broeikasgassen hoger dan ooit in de afgelopen 800, 000 jaar
Belangrijkste broeikasgassen hoger dan ooit in de afgelopen 800, 000 jaar Waar zijn op aarde tropische klimaten die het meest waarschijnlijk worden gevonden?
Waar zijn op aarde tropische klimaten die het meest waarschijnlijk worden gevonden?
Hoofdlijnen
- Nieuwe detectietechnieken kunnen droogtetolerantie in oude gewassen detecteren en kunnen nieuwe fokprogramma's informeren
- Het organel dat verantwoordelijk is voor afbraak van materiaal dat door endocytose in de cel in de cel wordt gebracht, is de?
- Zijn dinosaurussen echt? Wat we weten over de uitgestorven wezens
- Wat leven organismen in nauwe associatie met elkaar?
- Wat is het voordeel van fosforyleringscascade?
- Vasculaire planten: definitie, classificatie, kenmerken en voorbeelden
- Waarom kan een enkel cellen organisme zoals Paramecium buiten het lichaam overleven terwijl de menselijke cel zou sterven?
- Wat componeert DNA?
- Welke wetenschappelijke theorie zegt dat alle levende wezens bestaan uit cellen als levensfuncties en nieuwe cellen produceren?
- Nieuw inzicht brengt duurzame waterstof een stap dichterbij

- Nieuw materiaal breekt wereldrecord voor het omzetten van warmte in elektriciteit

- Muren bouwen die zomerse hittegolven draaglijker maken

- Metaalschuim houdt kogels van .50 kaliber tegen, evenals staal - bij minder dan de helft van het gewicht

- Metabolisch gemanipuleerde bacterie produceert luteïne
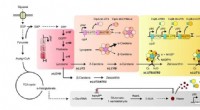
 Selectieve omzetting van CO₂ in dimethylether via hydrofobe en gallium-gemodificeerde koperkatalysatoren
Selectieve omzetting van CO₂ in dimethylether via hydrofobe en gallium-gemodificeerde koperkatalysatoren  Welk element heeft de letters AU als chemisch symbool?
Welk element heeft de letters AU als chemisch symbool?  Het ritme van verandering:wat een drumbeat-experiment onthult over culturele evolutie
Het ritme van verandering:wat een drumbeat-experiment onthult over culturele evolutie  Video:Wordt het kombucha?
Video:Wordt het kombucha? Wat verwijst naar de atmosferische omstandigheden op een bepaalde nacht?
Wat verwijst naar de atmosferische omstandigheden op een bepaalde nacht?  Wat is Lambda Max?
Wat is Lambda Max?  Ongecontroleerde raketafdalingen vormen een risico van 10% op het doden van een of meer mensen in de komende tien jaar
Ongecontroleerde raketafdalingen vormen een risico van 10% op het doden van een of meer mensen in de komende tien jaar Insecten vangen op kleur:zal het werken in Montana?
Insecten vangen op kleur:zal het werken in Montana?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

