
Wetenschap
Welk volume koolmonoxide bij STP is nodig om 541 ml dioxide te produceren?
1. Evenwichtige chemische vergelijking
De reactie die u beschrijft, is de verbranding van koolmonoxide:
2 CO (G) + O₂ (G) → 2 Co₂ (G)
2. Stoichiometrie
De gebalanceerde vergelijking vertelt ons dat 2 mol CO reageert om 2 mol co₂ te produceren. Dit betekent dat de molverhouding van CO tot co₂ 1:1 is.
3. Ideale gaswet
Bij STP (standaardtemperatuur en druk) bezet 1 mol ideaal gas 22,4 L. We kunnen deze informatie gebruiken om te converteren tussen volume en mollen.
4. Berekening
* Convert ML naar L: 541 ml co₂ =0,541 L co₂
* Bereken mol Co₂:
* (0,541 L co₂) / (22,4 l / mol) =0,0241 mol Co₂
* Aangezien de molverhouding 1:1 is, hebt u 0,0241 mol CO nodig.
* Bereken het volume van CO op STP:
* (0,0241 mol CO) * (22,4 l/mol) =0,540 l CO
* convert L naar ml: 0.540 L CO = 540 ml CO
Daarom heeft u 540 ml koolmonoxide bij STP nodig om 541 ml kooldioxide te produceren.
 Ongebalanceerde vergelijking voor vast zink plus zuurstof levert II-oxide op?
Ongebalanceerde vergelijking voor vast zink plus zuurstof levert II-oxide op?  Wat is de woordvergelijking wanneer magnesiumoxide ontstaat uit metaal en zuurstofgas?
Wat is de woordvergelijking wanneer magnesiumoxide ontstaat uit metaal en zuurstofgas?  Techniek kan helpen bij massaproductie van biologisch afbreekbaar plastic
Techniek kan helpen bij massaproductie van biologisch afbreekbaar plastic Een eenvoudige methode om vlakke microstructuren van polysiloxaan af te drukken
Een eenvoudige methode om vlakke microstructuren van polysiloxaan af te drukken De manier waarop een mineraal licht reflecteert, is het?
De manier waarop een mineraal licht reflecteert, is het?
 Evaluatie van op het land gebaseerde mitigatiestrategieën voor het bereiken van de klimaatdoelstellingen van 2°C
Evaluatie van op het land gebaseerde mitigatiestrategieën voor het bereiken van de klimaatdoelstellingen van 2°C  Geen goed nieuws hier:belangrijke IPCC-bevindingen over klimaatverandering
Geen goed nieuws hier:belangrijke IPCC-bevindingen over klimaatverandering Olie- en gasafvalwater als stofonderdrukker minder dan ideaal
Olie- en gasafvalwater als stofonderdrukker minder dan ideaal Grace opgewaardeerd tot orkaan, op weg naar Mexico
Grace opgewaardeerd tot orkaan, op weg naar Mexico Storm Nicholas verzwakt maar laat 450 achter, 000 huizen in Texas zonder stroom (update)
Storm Nicholas verzwakt maar laat 450 achter, 000 huizen in Texas zonder stroom (update)
Hoofdlijnen
- Hoeveel chromosomen zijn er in een van uw huidcellen?
- Hoe dieren getallen begrijpen, beïnvloedt hun overlevingskansen
- Genoomanalyse van vroege plantenafstamming werpt licht op hoe planten leerden te gedijen op het land
- Mariene wetenschappers leiden een uitgebreide beoordeling van soorten reuzenschelpdieren wereldwijd
- Zijn er subsystemen binnen het spijsverteringssysteem?
- Welk lichaamssysteem reguleert functies metabolisme?
- Waar coderen codons naast aminozuren voor?
- Wat is vergelijkbaar met het weefsel van de planten?
- Waarom wordt Grana keuken van de cel genoemd?
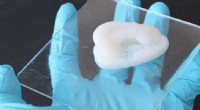
- Complexe objecten op cellulosebasis printen
- Onderzoekers krijgen een glimp op nanoschaal van spleet- en putcorrosie terwijl het gebeurt

- Kikkerschuim gebruiken als een antiseptisch toedieningssysteem

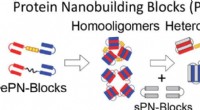
- Wetenschappers ontwikkelen eiwitten die zichzelf assembleren tot supramoleculaire complexen
- Legeronderzoek kijkt naar parels voor aanwijzingen voor het verbeteren van lichtgewicht bepantsering voor soldaten

 Worden fossielen gebruikt om sedimentaire rotsen te correleren die op grote schaal worden gescheiden door het onderscheidende fossiele gehalte te gebruiken en het principe van opvolging toe te passen?
Worden fossielen gebruikt om sedimentaire rotsen te correleren die op grote schaal worden gescheiden door het onderscheidende fossiele gehalte te gebruiken en het principe van opvolging toe te passen?  Uitvinding biedt nieuwe optie voor het bewaken van de gezondheid van het hart
Uitvinding biedt nieuwe optie voor het bewaken van de gezondheid van het hart Wat zijn de drie toepassingen van een permanente magneet?
Wat zijn de drie toepassingen van een permanente magneet?  Atomen in actie vangen:kijken naar next-gen materialen kristalliseren
Atomen in actie vangen:kijken naar next-gen materialen kristalliseren Converteer 6,55 maal 10 naar de 24e macht atomen koolstof mol koolstof?
Converteer 6,55 maal 10 naar de 24e macht atomen koolstof mol koolstof?  Een doorbraak in het monitoren van energieopslag op het werk met behulp van optische vezels
Een doorbraak in het monitoren van energieopslag op het werk met behulp van optische vezels Wat gebeurt er met de van alle kleuren als lichtgolven op een blauw object vallen?
Wat gebeurt er met de van alle kleuren als lichtgolven op een blauw object vallen?  Verplaatsing van gezondheidsgegevens van Google maakt wat misselijk
Verplaatsing van gezondheidsgegevens van Google maakt wat misselijk
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

