
Wetenschap
Wat zijn twee hoofdtypen elektronen en hoe ze diff?
Elektronen kunnen echter worden beschreven in verschillende staten Afhankelijk van hun energieniveau en locatie binnen een atoom:
1. gebonden elektronen: Deze elektronen worden geassocieerd met een atoom en zijn gebonden aan zijn kern door elektrostatische aantrekkingskracht. Ze bestaan in specifieke energieniveaus, orbitalen genoemd, die hun gedrag bepalen en bijdragen aan de chemische eigenschappen van het atoom.
2. Vrije elektronen: Deze elektronen zijn niet gebonden aan een bepaald atoom en kunnen vrij binnen een materiaal bewegen. Ze zijn verantwoordelijk voor elektrische geleidbaarheid in metalen en halfgeleiders.
Dit is hoe ze verschillen:
| Feature | Gebonden elektronen | Gratis elektronen |
| -------------- | ---------------------------------------------------------- | -------------------------------------------------------------- |
| Locatie | Rond de kern van een atoom | Vrij bewegen binnen een materiaal |
| Energieniveau | Bestaan in specifieke, gekwantiseerde energieniveaus | Kan een reeks energieniveaus bezitten |
| Beweging | Beperkt tot hun orbital | Kan door het materiaal bewegen, zelfs tegen een elektrisch veld |
| Rol | Bepaal de chemische eigenschappen van het atoom | Draag bij aan elektrische geleidbaarheid |
Dus hoewel er slechts één type elektron is, kunnen het gedrag en de rol ervan veranderen, afhankelijk van zijn toestand binnen een materiaal.
 NASA vindt weinig kracht meer in tropische cycloon Herold
NASA vindt weinig kracht meer in tropische cycloon Herold Meer dan een miljoen getroffen door moessonoverstromingen in India
Meer dan een miljoen getroffen door moessonoverstromingen in India Mensen vormen een steeds groter uitstervingsrisico voor dieren:beoordeling
Mensen vormen een steeds groter uitstervingsrisico voor dieren:beoordeling Door droogte getroffen Kaapstad moet buitenaardse bomen kappen:studie
Door droogte getroffen Kaapstad moet buitenaardse bomen kappen:studie Hé! Hè? Onderzoekers meten vakantiegevoel
Hé! Hè? Onderzoekers meten vakantiegevoel
Hoofdlijnen
- Wat zijn enkele stekelige planten die beginnen met de letter o?
- Hoe menselijk is onafhankelijkheid op biotische componenten?
- Wat is een levend organisme dat met uitsterven wordt bedreigd in zijn gehele of een aanzienlijk deel van zijn verspreidingsgebied?
- Biologen reizen met hun mobiele laboratorium om een breed scala aan mitochondriale functies bij vogelmigratie te bestuderen
- Komt ademhaling en fotosynthese beide voor in alle levende dingen?
- Waar komt al het goud vandaan?
- Wat zijn de twee soorten fermentatie en wat levert elk op?
- Wat zijn de eigenschappen van een enzym?
- Hoe veranderen mensen biomen en waarom wij dat?
- Onderzoeker verdiept zich in plaque-veroorzakende eiwitten bij ALS en dementie

- Bij longitudinaal onderzoek gedroogde bloedvlekmonsters spelen een rol
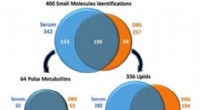
- Het ontdekken van nieuwe medicijnen is een lang en duur proces:chemische verbindingen die screeningtools misleiden, maken het nog moeilijker

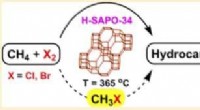
- De voetafdruk verkleinen van een broeikasgas dat krachtiger is dan koolstofdioxide
- Actieve machine learning voor de ontdekking en kristallisatie van gigantische polyoxometalaatmoleculen
 Veelzijdige lichtregeling in WSe₂ gerealiseerd
Veelzijdige lichtregeling in WSe₂ gerealiseerd  Kunstmatige fotosynthese stapt in het licht
Kunstmatige fotosynthese stapt in het licht Hubble is de ultieme multitasker:asteroïden ontdekken terwijl hij andere waarnemingen doet
Hubble is de ultieme multitasker:asteroïden ontdekken terwijl hij andere waarnemingen doet NASA vindt kracht in nieuwe tropische depressie in de Golf
NASA vindt kracht in nieuwe tropische depressie in de Golf Wat zit er in een NaCl -atoom?
Wat zit er in een NaCl -atoom?  Wat zijn de chemische verbindingen in een lippenstift?
Wat zijn de chemische verbindingen in een lippenstift?  Bijgewerkt Exascale-systeem voor simulaties op aarde is sneller dan zijn voorganger
Bijgewerkt Exascale-systeem voor simulaties op aarde is sneller dan zijn voorganger Protonmembranen samengesteld uit 2D gelaagde fosfor nanosheets
Protonmembranen samengesteld uit 2D gelaagde fosfor nanosheets
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

