
Wetenschap
Wat is het zwakste type binding en betrokken bij het binden van water?
Waterstofbinding is het zwakste type binding dat betrokken is bij het binden van water. Het is een intermoleculaire kracht die optreedt tussen een waterstofatoom dat covalent gebonden is aan een sterk elektronegatief atoom (zoals zuurstof, stikstof of fluor) en een ander elektronegatief atoom. In water vindt waterstofbinding plaats tussen de waterstofatomen van het ene watermolecuul en het zuurstofatoom van een ander watermolecuul. Dit type binding is verantwoordelijk voor de unieke eigenschappen van water, zoals de hoge oppervlaktespanning, de hoge specifieke warmtecapaciteit en het vermogen om veel stoffen op te lossen.
 Zeer selectieve membranen:onderzoekers ontdekken hoe water zijn eigen filtratie kan beïnvloeden
Zeer selectieve membranen:onderzoekers ontdekken hoe water zijn eigen filtratie kan beïnvloeden Hieronder ziet u een eiwitkanaal in een waterstofionenpomp?
Hieronder ziet u een eiwitkanaal in een waterstofionenpomp?  Een nieuwe generatie antimalariamiddelen
Een nieuwe generatie antimalariamiddelen Ultrasnelle elektronen in magnetische oxiden:een nieuwe richting voor spintronica?
Ultrasnelle elektronen in magnetische oxiden:een nieuwe richting voor spintronica? Echografieapparaat verbetert de oplaadtijd en gebruiksduur in lithiumbatterijen
Echografieapparaat verbetert de oplaadtijd en gebruiksduur in lithiumbatterijen
 Waarvoor wordt glucose gebruikt in een plant?
Waarvoor wordt glucose gebruikt in een plant?  Verminderde luchtvervuiling in de VS zal de regenval in de Sahel van Afrika stimuleren, zegt studie
Verminderde luchtvervuiling in de VS zal de regenval in de Sahel van Afrika stimuleren, zegt studie 3D-weergave van Amazonebossen legt de effecten van El Nino-droogte vast
3D-weergave van Amazonebossen legt de effecten van El Nino-droogte vast Liana's verstikken de fruit- en zaadproductie van bomen in tropische bossen
Liana's verstikken de fruit- en zaadproductie van bomen in tropische bossen Hoge CO2-niveaus kunnen mariene laagwolken destabiliseren
Hoge CO2-niveaus kunnen mariene laagwolken destabiliseren
Hoofdlijnen
- Waarom geven wetenschappers om wormen?
- Wat is innovatie, en hoe kunnen we de sluimerende eigenschappen ervan wakker schudden en cultiveren?
- Hoe houdt evolutie het creationisme in?
- Verrassend snelle evolutie waargenomen bij hagedissoorten
- Simpele microscoopexperimenten
- Hoe weeft een spin zijn web?
- Wat is de betekenis van de woorddelen pro en karyo. Hoe kunnen deze je helpen begrijpen wat een prokaryotische cel is?
- Ecologen zeggen dat het metabolisme de oorzaak is van het feit dat natuurlijke selectie slechts bepaalde soorten bevoordeelt
- Kunnen we 11 miljard mensen voeden en tegelijkertijd de verspreiding van infectieziekten voorkomen?
- Duurzame spuitbetonmix-ontwerpen voor tunnels met een langere levensduur

- Wetenschappers ontdekken nieuw bacterieel resistentiemechanisme tegen peptide-antibiotica
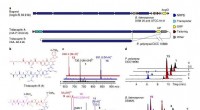
- Combinatie van microbiële en chemische vingerafdrukken voor forensische toepassingen

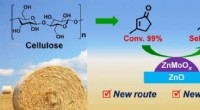
- Onderzoekers synthetiseren biobased methylcyclopentadieen met 3-methylcyclopent-2-enon
- Waterbehandeling:hormonen verwijderen met zonlicht

 De moderne mens ontstond meer dan 300, 000 jaar geleden, nieuwe studie suggereert:
De moderne mens ontstond meer dan 300, 000 jaar geleden, nieuwe studie suggereert: Man veroordeeld tot 15 jaar cel voor sabotage hacker
Man veroordeeld tot 15 jaar cel voor sabotage hacker EPA heeft het screeningsniveau voor lood in de bodem verlaagd:dit is wat dit zou kunnen betekenen voor huishoudens in de VS
EPA heeft het screeningsniveau voor lood in de bodem verlaagd:dit is wat dit zou kunnen betekenen voor huishoudens in de VS  Plakband voor waterdruppels bootst rozenblaadjes na
Plakband voor waterdruppels bootst rozenblaadjes na Hogere temperaturen betekenen hogere voedsel- en andere prijzen. Een nieuwe studie koppelt klimaatschokken aan inflatie
Hogere temperaturen betekenen hogere voedsel- en andere prijzen. Een nieuwe studie koppelt klimaatschokken aan inflatie  Wetenschappers laten zien dat kwantum-infraroodspectroscopie ultrabreedbandspectroscopiemetingen kan uitvoeren
Wetenschappers laten zien dat kwantum-infraroodspectroscopie ultrabreedbandspectroscopiemetingen kan uitvoeren  Een manier om batterijen in bijna elke gewenste vorm te maken
Een manier om batterijen in bijna elke gewenste vorm te maken Interventie met kamerplanten:nieuwe antwoorden voor het ontwerp van de gezondheidszorg?
Interventie met kamerplanten:nieuwe antwoorden voor het ontwerp van de gezondheidszorg?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

