
Wetenschap
Reactie van ammoniumchloride en zilvernitraat:evenwichtige vergelijking en uitleg
NH₄Cl(aq) + AgNO₃(aq) → AgCl(s) + NH₄NO₃(aq)
Hier is een overzicht van de reactie:
* Reactanten:
* Ammoniumchloride (NH₄Cl) is een kleurloze ionische verbinding.
* Zilvernitraat (AgNO₃) is ook een kleurloze ionische verbinding.
* Producten:
* Zilverchloride (AgCl) is een witte, onoplosbare vaste stof die uit de oplossing neerslaat.
* Ammoniumnitraat (NH₄NO₃) is een kleurloze ionische verbinding die opgelost blijft in de oplossing.
Uitleg:
Deze reactie is een dubbele verplaatsingsreactie, wat betekent dat de positieve en negatieve ionen van partner wisselen. De zilverionen (Ag⁺) uit zilvernitraat reageren met de chloride-ionen (Cl⁻) uit ammoniumchloride en vormen zilverchloride (AgCl), dat onoplosbaar is in water en een wit neerslag vormt. De ammoniumionen (NH₄⁺) en nitraationen (NO₃⁻) blijven in oplossing als ammoniumnitraat (NH₄NO₃).
Belangrijkste punten:
* De reactie is gebalanceerd, wat betekent dat er aan beide kanten van de vergelijking gelijke aantallen van elk type atoom zijn.
* De statussymbolen geven de fysieke toestand van elke stof aan:(aq) voor waterig (opgelost in water) en (s) voor vast.
*Deze reactie kan worden gebruikt om te testen op de aanwezigheid van chloride-ionen in een oplossing.
 Nieuw geautomatiseerd vulkaanwaarschuwingssysteem voorspelt dreigende uitbarstingen
Nieuw geautomatiseerd vulkaanwaarschuwingssysteem voorspelt dreigende uitbarstingen Hoge concentraties gefluoreerde chemische stof GenX gevonden in stroomgebied
Hoge concentraties gefluoreerde chemische stof GenX gevonden in stroomgebied Extreem smeltseizoen leidt tot decennialange ecosysteemveranderingen in de poolwoestijn van Antarctica
Extreem smeltseizoen leidt tot decennialange ecosysteemveranderingen in de poolwoestijn van Antarctica Geologen graven in de mysterieuze kloof van Grand Canyons in de tijd
Geologen graven in de mysterieuze kloof van Grand Canyons in de tijd Uitbreiding van cannabisgewas naar bossen bedreigt leefgebied voor wilde dieren, veroorzaakt andere milieuschade
Uitbreiding van cannabisgewas naar bossen bedreigt leefgebied voor wilde dieren, veroorzaakt andere milieuschade
Hoofdlijnen
- Waarom natuurlijke netwerken stabieler zijn dan door de mens gemaakte netwerken
- Wetenschappers geven 's werelds eerste DNA-kaart van een bedreigde Australische muis vrij, en het zal helpen om deze te redden
- Welk organisme levert materie en energie?
- Heeft Archaea een celmembraan?
- Wat zijn de componenten van een eicellen?
- Welke factoren beïnvloeden het waterpotentieel in levende cellen?
- Wat is een milkweed -product?
- Reptielenzenuwstelsel:structuur en functie - een uitgebreide gids
- Welke organismen kunnen niet zowel seksueel als aseksueel reproduceren?
- De slingpsychrometer onder de knie krijgen:stapsgewijze handleiding voor het meten van de vochtigheid en het dauwpunt

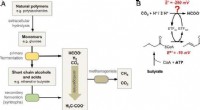
- Cruciale stap geïdentificeerd in de omzetting van biomassa naar methaan
- Afgedankt afval kan een schat aan zeldzame metalen zijn

- Chemici bedenken een manier om microplastics te verwijderen met okra

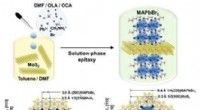
- Onconventioneel oplossingsproces voor 2-D heterostructuur
 Turbulente tijdperk leidde tot sprong in menselijk gedrag, aanpassingsvermogen 320, 000 jaar geleden
Turbulente tijdperk leidde tot sprong in menselijk gedrag, aanpassingsvermogen 320, 000 jaar geleden Wat vertegenwoordigt het subscript van de chemische formule ammoniak in de wetenschap?
Wat vertegenwoordigt het subscript van de chemische formule ammoniak in de wetenschap?  Nieuwe NASA X-plane constructie begint nu
Nieuwe NASA X-plane constructie begint nu Lang leve Nemo! Nieuw diermodel in verouderingsonderzoek?
Lang leve Nemo! Nieuw diermodel in verouderingsonderzoek?  Fluctuerende koffieprijzen oefenen mentale druk uit op Vietnamese boeren
Fluctuerende koffieprijzen oefenen mentale druk uit op Vietnamese boeren  Wie heeft de magneet gevonden?
Wie heeft de magneet gevonden?  Hoe weet je of je plant rasechte en hybride is?
Hoe weet je of je plant rasechte en hybride is?  Kunnen walkies vertellen wie de leider van de roedel is?
Kunnen walkies vertellen wie de leider van de roedel is?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

