
Wetenschap
Bijtende soda om zoutzuur te neutraliseren:berekening en gids
* Concentratie van het zoutzuur: Dit wordt uitgedrukt in eenheden zoals molariteit (mol per liter) of normaliteit (equivalenten per liter).
* Volume van het zoutzuur: Dit is de hoeveelheid HCl-oplossing die u wilt neutraliseren.
Zo berekent u de benodigde hoeveelheid bijtende soda:
1. Schrijf de uitgebalanceerde chemische vergelijking:
NaOH + HCl → NaCl + H₂O
2. Bepaal het aantal mol HCl:
* Vermenigvuldig de concentratie HCl met het volume HCl.
*Als je bijvoorbeeld 1 liter 1 M HCl hebt, heb je 1 mol HCl.
3. Bereken het aantal benodigde mol NaOH:
* De uitgebalanceerde vergelijking toont een molverhouding van 1:1 tussen NaOH en HCl. Dit betekent dat je evenveel mol NaOH nodig hebt als het aantal mol HCl.
4. Omzetten van mol NaOH naar grammen:
* Vermenigvuldig het aantal mol NaOH met de molmassa van NaOH (40 g/mol).
Voorbeeld:
Stel dat u 250 ml 0,5 M HCl heeft en dit wilt neutraliseren met NaOH.
1. Molen HCl: 0,25 L * 0,5 mol/L =0,125 mol HCl
2. Molen NaOH nodig: 0,125 mol NaOH
3. Gram NaOH nodig: 0,125 mol * 40 g/mol =5 gram NaOH
Belangrijke opmerking: Deze berekening gaat uit van volledige neutralisatie. In praktijkscenario's is het vaak het beste om een kleine overmaat NaOH te gebruiken om volledige neutralisatie te garanderen en om mogelijke verliezen op te vangen.
 Wat moet je voordat je iets als theorie in de wetenschap claimt?
Wat moet je voordat je iets als theorie in de wetenschap claimt?  Bedreigde flora op de Filipijnen:97 bedreigde soorten
Bedreigde flora op de Filipijnen:97 bedreigde soorten  Supertyfoon Tramis-regenval onderzocht door NASA / JAXAs GPM-satelliet
Supertyfoon Tramis-regenval onderzocht door NASA / JAXAs GPM-satelliet Twee significante opwarmingsintervallen in Zuid-China sinds 1850
Twee significante opwarmingsintervallen in Zuid-China sinds 1850 Onderzoeker vindt goedkope manier om invasieve kokosnoten vanuit de ruimte te identificeren
Onderzoeker vindt goedkope manier om invasieve kokosnoten vanuit de ruimte te identificeren
Hoofdlijnen
- Is het een jongen of is het een meisje? Nieuwe methode om het geslacht van babyzeeschildpadden te identificeren
- Wat is een bioswale?
- Bevat de blauwdrukken van cel?
- Een chimpansee-varken hybride oorsprong voor mensen?
- Hoe heeft schimmels een speciale manier om te verhuizen?
- De krimpende eland van Isle Royale
- Zijn enzymen slechts een kleine minderheid van cellulaire massa uit?
- Welke belangrijke morfologie -functie wordt gebruikt om organismen als zoogdieren te classificeren?
- Wat is het cluster van cellen die een zich ontwikkelende ei omringen in eierstok genoemd?
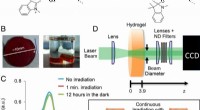
- Een nieuw licht schijnen op biomimetische materialen
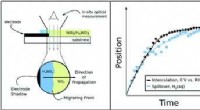
- Nieuwe aanpak creëert een uitzonderlijke katalysator met één atoom voor watersplitsing

- Hernieuwbare elektriciteit gebruiken voor industriële hydrogeneringsreacties
- Nanocapsules maken cel-geïnspireerde metabolische reacties mogelijk

- Hydrogel baant weg voor biomedische doorbraak

 Een nieuwe studie toont aan dat mieren voor de verstandigere optie kiezen, zelfs als dat betekent dat je wat harder moet werken
Een nieuwe studie toont aan dat mieren voor de verstandigere optie kiezen, zelfs als dat betekent dat je wat harder moet werken Waar zijn ontleders op de energiepiramide?
Waar zijn ontleders op de energiepiramide?  Wat als er geen Google was?
Wat als er geen Google was?  Wat is de tempituer van het centrum van de aarde?
Wat is de tempituer van het centrum van de aarde?  Wormgenomen onthullen een verband tussen mensen en verre verwanten
Wormgenomen onthullen een verband tussen mensen en verre verwanten Wat is de methode voor het opnemen van locatiesterren?
Wat is de methode voor het opnemen van locatiesterren?  Wat gebeurt er als de twee gevaarlijke elementen kalium en chloor worden gecombineerd?
Wat gebeurt er als de twee gevaarlijke elementen kalium en chloor worden gecombineerd?  Wat is de moleculaire formule van jodium?
Wat is de moleculaire formule van jodium?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

