
Wetenschap
Koolmonoxide in water:oplosbaarheid, reacties en evenwicht
* Lage oplosbaarheid: CO is slechts in geringe mate oplosbaar in water. Dit betekent dat er op elk moment slechts een kleine hoeveelheid CO oplost.
* Geen significante chemische reactie: CO reageert niet significant met water om nieuwe chemische soorten te vormen. In tegenstelling tot gassen zoals kooldioxide (CO2), die koolzuur (H2CO3) in water vormen, ondergaat CO geen soortgelijke reactie.
* Evenwicht: Het opgeloste CO bestaat in evenwicht met CO in de gasfase. Naarmate de concentratie CO in het water afneemt, zal meer CO uit de gasfase oplossen om het evenwicht te herstellen.
De interactie van CO met water is echter niet geheel te verwaarlozen:
* Hemoglobinebinding: Het is bekend dat CO zich aan hemoglobine in het bloed bindt, zelfs als het in water is opgelost. Deze binding is veel sterker dan de binding van zuurstof aan hemoglobine, wat leidt tot koolmonoxidevergiftiging.
* Potentieel voor hydrolyse: Onder extreem specifieke omstandigheden kan CO reageren met water in de aanwezigheid van sterke katalysatoren, maar dit komt niet vaak voor.
Samengevat: Hoewel CO in kleine mate in water oplost, is de interactie met water zwak en resulteert deze niet in significante chemische reacties. Het meest opvallende gevolg van het oplossen van CO in water is het vermogen ervan om zich aan hemoglobine te binden en vergiftiging te veroorzaken.
 Niet -cyclische elektronenstroom resulteert in het genereren van wat?
Niet -cyclische elektronenstroom resulteert in het genereren van wat?  Het volume chloorgas berekenen:een stapsgewijze handleiding
Het volume chloorgas berekenen:een stapsgewijze handleiding  Wat houden de moleculen in een vloeistof bij elkaar?
Wat houden de moleculen in een vloeistof bij elkaar?  Zal een katalysator de reactie van de reactie in de chemische reactie veranderen?
Zal een katalysator de reactie van de reactie in de chemische reactie veranderen?  Elementen aan weerszijden van het periodiek systeem?
Elementen aan weerszijden van het periodiek systeem?
 Wiskundige innovaties maken vooruitgang in de detectie van seismische activiteiten mogelijk
Wiskundige innovaties maken vooruitgang in de detectie van seismische activiteiten mogelijk  NASA ziet tyfoon Bavi op een miljoen mijl afstand
NASA ziet tyfoon Bavi op een miljoen mijl afstand Op zoek naar de sleutel om 20 dagen van tevoren hittegolven boven het stroomgebied van de Yangtze-rivier te voorspellen
Op zoek naar de sleutel om 20 dagen van tevoren hittegolven boven het stroomgebied van de Yangtze-rivier te voorspellen Waarom kan vegetatie worden gebruikt om klimaatgrenzen te helpen definiëren?
Waarom kan vegetatie worden gebruikt om klimaatgrenzen te helpen definiëren?  Attributiewetenschap zegt dat klimaatverandering verantwoordelijk is voor sommige extreme weersomstandigheden
Attributiewetenschap zegt dat klimaatverandering verantwoordelijk is voor sommige extreme weersomstandigheden
Hoofdlijnen
- Wat zijn de drie concepten waaruit de celtheorie bestaat?
- Wat is er tussen de pubis en ischium?
- Wat zijn bloedstollingseiwitten?
- Hoe is milkweed belangrijk voor vlinders?
- Welke van de volgende technologieën opende een nieuwe takwetenschap in de jaren 1970 A. Lichtmicroscoop B. Veranderende genen Bacteriën C. Centrifuge D. Chromatografie?
- Archeologie en ecologie geven samen een vollediger beeld van vroegere relaties tussen mens en natuur
- Hoe zoologie is gerelateerd aan de biologie?
- Vertegenwoordigt Cell City een plant of een dier uit?
- Eerste levensvormen op aarde onthuld in hete lente
- Glycanen als biomarkers voor kanker?
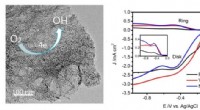
- Nieuwe elektrokatalysator ontwikkeld voor zuurstofreductiereactie
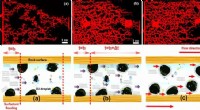
- Gebouwen:de onbreekbare band

- Stapsgewijze handleiding voor het thuis looien van schapenhuiden

- Een nieuwe klasse vertakte oppervlakteactieve stoffen met enkele keten voor verbeterde oliewinning gerapporteerd
 Welke bal bonces hoger de golf- of piepschuimbal?
Welke bal bonces hoger de golf- of piepschuimbal?  Rust biedt een goedkope manier om met arseen vergiftigd water te filteren
Rust biedt een goedkope manier om met arseen vergiftigd water te filteren Welk fysiek kenmerk heeft de plantachtige Noctiluca en Animalle -Trypanosoma Gambienese gemeen?
Welk fysiek kenmerk heeft de plantachtige Noctiluca en Animalle -Trypanosoma Gambienese gemeen?  Waarmee vergelijkde Carl Sagan de sterren mee?
Waarmee vergelijkde Carl Sagan de sterren mee?  Welke twee factoren bepalen momentum a. Massasnelheid b. kracht c. versnelling i. en zwaartekracht?
Welke twee factoren bepalen momentum a. Massasnelheid b. kracht c. versnelling i. en zwaartekracht?  Wat betekent de BRIX -zuurverhouding in sap?
Wat betekent de BRIX -zuurverhouding in sap?  Jupiter zou een ideale detector voor donkere materie kunnen zijn
Jupiter zou een ideale detector voor donkere materie kunnen zijn Wat zijn de negatieve effecten van hybridisatie?
Wat zijn de negatieve effecten van hybridisatie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

