
Wetenschap
Welke verklaring legt uit waarom lage temperatuur en hoge druk vereist zijn om chloorgas vloeibaar te maken?
Het verlagen van de temperatuur vermindert de kinetische energie van de gasmoleculen, waardoor ze dichter bij elkaar kunnen komen. Het vergroten van de druk dwingt de moleculen dichter bij elkaar en overwinnen hun natuurlijke neiging om zich te verspreiden.
Dit is waarom:
* lage temperatuur: Bij hoge temperaturen hebben gasmoleculen veel kinetische energie en bewegen ze snel, waardoor het voor hen moeilijk is om te condenseren. Het verlagen van de temperatuur vermindert hun kinetische energie, waardoor ze langzamer bewegen en minder vaak botsen. Hierdoor kunnen intermoleculaire krachten van kracht worden en de moleculen samen aantrekken.
* Hoge druk: Het vergroten van de druk dwingt de gasmoleculen dichter bij elkaar, waardoor de ruimte tussen hen wordt verminderd. Deze verhoogde nabijheid stelt intermoleculaire krachten in staat om belangrijker te worden, wat opnieuw bijdraagt aan het condensatieproces.
In wezen werken lage temperatuur en hoge druk synergetisch om de kinetische energie van de moleculen te verminderen en de kans dat ze intermoleculaire bindingen vormen, te vergroten, wat leidt tot vloeibaarmaking.
 Vergroening van biomaterialen en steigers die worden gebruikt in regeneratieve geneeskunde
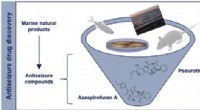
Vergroening van biomaterialen en steigers die worden gebruikt in regeneratieve geneeskunde Veelbelovende antikankermolecuul geïdentificeerd
Veelbelovende antikankermolecuul geïdentificeerd Wat is de juiste naam voor samengestelde COCL3?
Wat is de juiste naam voor samengestelde COCL3?  Onderzoekers maken doorbraak in antioxidant-enzym gekoppeld aan geelzucht
Onderzoekers maken doorbraak in antioxidant-enzym gekoppeld aan geelzucht Weet jij de weg naar Berkelium, Californië?
Weet jij de weg naar Berkelium, Californië?
Hoofdlijnen
- Stappen van DNA-transcriptie
- Een methode met wortels in AI legt bloot hoe mensen keuzes maken in groepen en sociale media
- Wat omvat osmose?
- Wat de mechanische krachten achter de eiwitvouwing ons kunnen vertellen over uitgezaaide kanker
- Wiskunde laat zien hoe ziekten zich ontwikkelen en hoe bacteriën resistentie tegen geneesmiddelen ontwikkelen
- Waarom is een voedselweb een realistischere manier om een ecosysteem af te beelden dan keten?
- Welke soorten wereldwijde veranderingen betreffen biologen?
- Hoe dragen dieren zoals het afgebeelde hert bij aan de stikstofcyclus?
- Wie is er begonnen met de wetenschap?
- Edelmetaalclusters kunnen de prestaties van katalysatoren verbeteren en hulpbronnen besparen

- 3D-printen verandert nanomachines in levensgrote arbeiders

- Schimmel Rode Zee levert aanknopingspunten voor nieuwe medicijnen tegen epilepsie
- Plantaardige eiwitten uitdrogen met de snelheid van het geluid

- Forensisch chemicus detecteert marihuanagebruik op basis van zweettest

 Wat is het verschil tussen Caves Rock Shelter and Houses?
Wat is het verschil tussen Caves Rock Shelter and Houses?  Iron Man-achtige exoskeletten bestudeerd om de productiviteit te verbeteren, veiligheid, en welzijn
Iron Man-achtige exoskeletten bestudeerd om de productiviteit te verbeteren, veiligheid, en welzijn Hoeveel pond zijn er in 41 mg?
Hoeveel pond zijn er in 41 mg?  Dankzij extra grote 'atomen' kunnen natuurkundigen van Penn het raadsel oplossen waarom dingen smelten
Dankzij extra grote 'atomen' kunnen natuurkundigen van Penn het raadsel oplossen waarom dingen smelten  Welke structuren gaan uit elkaar tijdens mitose en creëren spil?
Welke structuren gaan uit elkaar tijdens mitose en creëren spil?  Bewijs voor anisotropie van kosmische versnelling
Bewijs voor anisotropie van kosmische versnelling Het geheime leven van kreeft (handel):Kunnen we in heet water zitten?
Het geheime leven van kreeft (handel):Kunnen we in heet water zitten?  Seleniumankers kunnen de duurzaamheid van platinabrandstofcelkatalysatoren verbeteren
Seleniumankers kunnen de duurzaamheid van platinabrandstofcelkatalysatoren verbeteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

