
Wetenschap
Bij STP 0,250L van een onbekend gas heeft een massa 1,00 gram. Bereken zijn molaire massa.?
1. Begrijp de concepten
* Molaire massa: De massa van één mol van een stof (gram per mol, g/mol).
* STP (standaardtemperatuur en druk): 0 ° C (273,15 K) en 1 atm druk.
* Ideale gaswet: Pv =nrt, waar:
* P =druk (atm)
* V =volume (l)
* n =aantal mol
* R =ideale gasconstante (0,0821 l⋅atm/mol⋅k)
* T =temperatuur (k)
2. Bereken mol (n)
* Gebruik de ideale gaswet om het aantal mol (n) van het gas te vinden:
* n =pv / rt
* n =(1 atm) (0,250 l) / (0,0821 l⋅atm / mol⋅K) (273,15 k)
* n ≈ 0,0110 mol
3. Molaire massa berekenen
* Molaire massa (m) is massa (m) gedeeld door mol (n):
* M =m / n
* M =1,00 g / 0,0110 mol
* M ≈ 90,9 g/mol
Daarom is de molaire massa van het onbekende gas ongeveer 90,9 g/mol.
 Kunnen we erop vertrouwen dat studenten gegevens verzamelen die klaar zijn voor wetenschappelijk onderzoek?
Kunnen we erop vertrouwen dat studenten gegevens verzamelen die klaar zijn voor wetenschappelijk onderzoek?  Is kalium reactiever dan jodium?
Is kalium reactiever dan jodium?  Wat is een strass?
Wat is een strass?  Welke soorten intermoleculaire krachten zijn aanwezig in een mengsellithiumfosfaat en methanol (CH3OH)?
Welke soorten intermoleculaire krachten zijn aanwezig in een mengsellithiumfosfaat en methanol (CH3OH)?  Wat is het proces dat moleculen aan elkaar bindt?
Wat is het proces dat moleculen aan elkaar bindt?
 Californië bosbrand fakkelt bos, dwingt nieuwe evacuaties af
Californië bosbrand fakkelt bos, dwingt nieuwe evacuaties af Hoe India's 'krottenwijkvrije' herontwikkeling de bewoners in de steek laat door hun ontwerpinzichten en -behoeften te negeren
Hoe India's 'krottenwijkvrije' herontwikkeling de bewoners in de steek laat door hun ontwerpinzichten en -behoeften te negeren  tegen 2100, oceanen kunnen genoeg koolstof bevatten om de zesde massale uitroeiing van soorten te starten, wiskunde voorspelt (Update)
tegen 2100, oceanen kunnen genoeg koolstof bevatten om de zesde massale uitroeiing van soorten te starten, wiskunde voorspelt (Update) NASA vindt sterkste stormen buiten het centrum in Tropical Storm 14W
NASA vindt sterkste stormen buiten het centrum in Tropical Storm 14W Hoe beïnvloedt klimaatverandering biodiversiteit?
Hoe beïnvloedt klimaatverandering biodiversiteit?
Hoofdlijnen
- Heeft de toegenomen genduplicatie de weg geëffend voor de menselijke evolutie?
- Tabaksplanten als levensredders
- Wat is de toniciteit van de cel?
- Wat is de geschatte efficiëntie van cellulaire ademhaling voor een mutant organisme dat slechts 29 mol ATP produceert elke mol glucose geoxideerd in plaats van normaal 36 - 38 ATP?
- Hoe bacteriën hun motoren turbochargeerden
- Waarom zijn Endospores een belangrijke overweging voor de conservenindustrie?
- Wetenschappers vragen zich af:hoe kunnen vloeibare organellen in cellen naast elkaar bestaan zonder te fuseren?
- Onderzoekers ontdekken door het meten van krachten hoe het darmepitheel vouwt en beweegt
- Bestaat er echt een ‘mama’-gen bij vrouwen?
- Wetenschappers onthullen hoe wasmiddelen eigenlijk werken
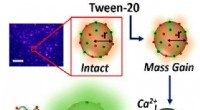
- Biologisch materiaal verhoogt de prestaties van zonnecellen

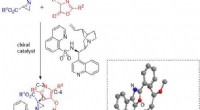
- Door koper gekatalyseerde enantioselectieve trifluormethylering van benzylische radicalen ontwikkeld

- Asymmetrische synthese van aziridine met een nieuwe katalysator kan helpen bij de ontwikkeling van nieuwe medicijnen
- Spinchemicaliën voor snellere reacties

 Turbulentie verwondt 30 gewonden op vlucht van Istanbul naar New York
Turbulentie verwondt 30 gewonden op vlucht van Istanbul naar New York Bevroren bezittingen:wie krijgt de embryo’s als een koppel uit elkaar gaat?
Bevroren bezittingen:wie krijgt de embryo’s als een koppel uit elkaar gaat?  Wat gebeurt er als je een bal in de ruimte gooit?
Wat gebeurt er als je een bal in de ruimte gooit?  Isoleert het het axon van neuron?
Isoleert het het axon van neuron?  Machine learning-methode voorspelt nauwkeurig metaaldefecten
Machine learning-methode voorspelt nauwkeurig metaaldefecten Heeft meervoudig onverzadigde vetten minder waterstofatomen dan verzadigde vetten?
Heeft meervoudig onverzadigde vetten minder waterstofatomen dan verzadigde vetten?  Lichtflitsen op de donkere materie
Lichtflitsen op de donkere materie Nieuw onderzoek laat zien hoe klimaatverandering de impact van rondwormen op graslanden kan beïnvloeden
Nieuw onderzoek laat zien hoe klimaatverandering de impact van rondwormen op graslanden kan beïnvloeden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

