
Wetenschap
Polaire covalente bindingen begrijpen:elektronegativiteit uitgelegd
1. Wat is elektronegativiteit?
* Elektronegativiteit is het vermogen van een atoom om elektronen naar zich toe te trekken in een chemische binding. Het is een maatstaf voor hoe sterk een atoom een elektron "wil" verwerven.
* Atomen met een hogere elektronegativiteit hebben een sterkere aantrekkingskracht op gedeelde elektronen.
2. Polaire covalente obligaties:ongelijk delen
* Wanneer twee atomen verschillend zijn elektronegativiteiten vormen een binding, de elektronen worden niet gelijk verdeeld.
* Het atoom met een hogere elektronegativiteit zal de gedeelde elektronen sterker aantrekken, waardoor een gedeeltelijke negatieve lading ontstaat (δ-) op dat atoom.
* Het andere atoom, met een lagere elektronegativiteit, zal een gedeeltelijk positieve lading hebben (δ+).
* Deze ongelijke verdeling van elektronen leidt tot een polaire covalente binding .
3. Visualisatie:
Stel je een touwtrekken voor tussen twee atomen met verschillende sterktes. Het sterkere atoom (hogere elektronegativiteit) trekt het touw (elektronen) dichter naar zich toe, waardoor een lichte onbalans in de verdeling van het touw ontstaat.
4. Voorbeeld:Water (H₂O)
*Zuurstof (O) heeft een hogere elektronegativiteit dan waterstof (H).
* In een watermolecuul trekt het zuurstofatoom de gedeelde elektronen dichter naar zich toe, waardoor het enigszins negatief wordt (δ-).
* De waterstofatomen worden lichtjes positief (δ+).
* Deze ongelijkmatige ladingsverdeling maakt het watermolecuul polair.
Belangrijkste punten:
* Een significant verschil in elektronegativiteit is vereist om een polaire covalente binding te vormen.
* Hoe groter het verschil , hoe polairder de binding.
* Polaire covalente bindingen zijn verantwoordelijk voor veel belangrijke eigenschappen van moleculen, zoals het vermogen van water om veel stoffen op te lossen.
Laat het me weten als je meer voorbeelden of een diepere uitleg van een onderdeel wilt!
 NASA ontdekt dat het metrogebied van Virginia ongelijk aan het zinken is
NASA ontdekt dat het metrogebied van Virginia ongelijk aan het zinken is Wereldtemperaturen van de afgelopen 24.000 jaar laten een ongekende opwarming van vandaag zien
Wereldtemperaturen van de afgelopen 24.000 jaar laten een ongekende opwarming van vandaag zien Wat is betekenis in wetenschap en geschiedenis?
Wat is betekenis in wetenschap en geschiedenis?  Wat zijn de milieutinten van groen?
Wat zijn de milieutinten van groen?  Zonlicht en plantengroei:inzicht in de vitale verbinding
Zonlicht en plantengroei:inzicht in de vitale verbinding
Hoofdlijnen
- Hoe kunnen mensen profiteren van de verschillende delen van een plant?
- Waarom is de operon gebruikelijk in prokaryoten, niet in eukaryoten?
- Wat is een biota?
- Hoe groeien en verspreiden micro -organismen zich zo snel?
- Onderzoek naar hoe genen activeren levert verrassende ontdekkingen op
- Wat zijn redenen waarom eukaryotische cellen zich verdelen?
- Voor- en nadelen van recombinant-DNA-technologie:een evenwichtig overzicht
- De plantencelkern:het controlecentrum van de cel begrijpen
- Interacties tussen eenvoudige moleculaire mechanismen leiden tot complexe infectiedynamiek
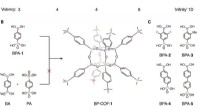
- Nieuw covalent organisch raamwerk met boor en fosfor zorgt voor betere connectiviteit
- Nanokristallijne materialen met verminderde zuurstof vertonen verbeterde prestaties

- Olie opruimen met magneten
- Kunstmatige intelligentie kan wetenschappers helpen bij het maken van spray-on zonnecellen

- Hoe een chemische oplossing te concentreren door eenvoudige destillatie

 Naar huis bellen? Ily vindt de vaste lijn opnieuw slimmer en gebruiksvriendelijker
Naar huis bellen? Ily vindt de vaste lijn opnieuw slimmer en gebruiksvriendelijker  De milieu-impact van de wereldwijde gebouwde omgevingssector verminderen
De milieu-impact van de wereldwijde gebouwde omgevingssector verminderen Wat eronder ligt
Wat eronder ligt  Datasoftwarebedrijf Snowflake landt op Microsofts Azure-cloud
Datasoftwarebedrijf Snowflake landt op Microsofts Azure-cloud Is het mogelijk om energie te vernietigen of te creëren?
Is het mogelijk om energie te vernietigen of te creëren?  Hoe piekfaciliteiten de tijd tot hereniging voor niet-begeleide migrantenkinderen en hun families beïnvloedden
Hoe piekfaciliteiten de tijd tot hereniging voor niet-begeleide migrantenkinderen en hun families beïnvloedden  Een nieuwe tool voor datawetenschappers en biologen en meer
Een nieuwe tool voor datawetenschappers en biologen en meer Cephalization of Earthworms
Cephalization of Earthworms
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

